
| A. | 1 mol R(g)的能量总和大于1 mol M(s)与1 mol N(g) 的能量总和 | |
| B. | 将2 mol R (g)与1 mol N(g)在该条件下充分反应,放出热量Q2 kJ | |
| C. | 当1 mol M(s) 与N(g)完全转化为T (g)时(假定无热量损失),放出热量Q1+$\frac{{Q}_{2}}{2}$kJ | |
| D. | M(g)+N(g)?R(g)△H=-Q3 kJ•mol-1,则Q3<Q1 |
分析 A、反应焓变为负值,反应是放热反应,反应物能量高于生成物;
B、反应是可逆反应不能进行彻底;
C、依据热化学方程式和盖斯定律计算分析判断;
D、固体变化为气体吸收能量,反应是放热反应焓变为负值.
解答 解:A、反应焓变为负值,反应是放热反应,反应物能量高于生成物,1mol R(g)的能量总和小于1mol M(s)与1mol N(g)的能量总和,故A错误;
B、反应是可逆反应不能进行彻底,将2mol R(g)与1mol N(g)在该条件下充分反应,放出热量<Q2 kJ,故B错误;
C、依据热化学方程式和盖斯定律计算分析判断,①+$\frac{②}{2}$得到,M(s)+$\frac{3}{2}$N(g)?T(g)△H=-(Q1+$\frac{{Q}_{2}}{2}$)kJ/mol,则C正确;
D、固体变化为气体吸收能量,反应是放热反应焓变为负值,M(g)+N(g)?R(g)△H=-Q3 kJ•mol-1,则Q3>Q1,故D错误;
故选C.
点评 本题考查了化学反应能量变化,盖斯定律计算应用,注意焓变为负值是放热反应,题目难度中等.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | 全氟丙烷不能使溴水褪色 | |
| B. | 全氟丙烷的电子式为: | |
| C. | 相同压强下,沸点:C3F8<C3H8 | |
| D. | 分子中三个碳原子可能处于同一直线上 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 16g CH4中含有4NA个C-H键 | |
| B. | 1mol•L-1NaCl溶液含有NA个Na+ | |
| C. | 1 L 0.1 mol•L-1盐酸含有0.1NA个HCl分子 | |
| D. | 1mol Cl2与足量的铁反应,转移的电子总数为2NA个 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
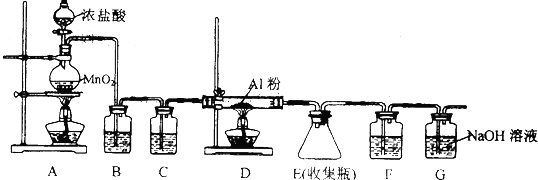
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

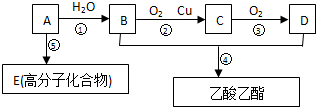
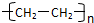

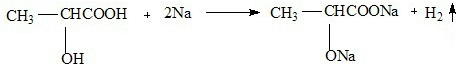 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将SO2通入溴水,溴水褪色 | |
| B. | 将SO2气体通入滴入有酚酞的NaOH溶液中,红色褪色 | |
| C. | 将SO2通入品红溶液中,品红溶液褪色 | |
| D. | 将SO2通入酸性高锰酸钾溶液中,溶液褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②③ | B. | ①② | C. | ①③ | D. | ①②③ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com