
 能源问题是当代社会面临的重大课题,甲醇是未来的重要能源物质.合成甲醇的反应为:CO(g)+2H2(g)?CH3OH(g).
能源问题是当代社会面临的重大课题,甲醇是未来的重要能源物质.合成甲醇的反应为:CO(g)+2H2(g)?CH3OH(g). CH3OH(g);
CH3OH(g);

科目:高中化学 来源: 题型:
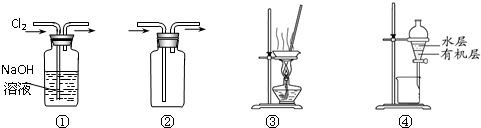
| A、装置①可用于除去Cl2中含有的少量HCl气体 |
| B、按装置②所示的气流方向可用于收集H2、NH3等 |
| C、用图③所示装置蒸干NH4Cl饱和溶液制备NH4Cl晶体 |
| D、用图④所示装置分离CCl4萃取碘水后已分层的有机层和水层 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、向酸化的FeSO4中加入H2O2溶液:2Fe2++2H++H2O2═2Fe3++2H2O |
| B、向NaHCO3溶液中加入足量Ba(OH)2的溶液:Ba2++2HCO3-+2OH-═2H2O+BaCO3↓+CO32- |
| C、向苯酚钠溶液中通入少量的CO2:2C6H5O-+CO2+H2O═2C6H5OH+CO32- |
| D、向NaOH溶液中滴加少量氯化铝溶液:Al(OH)3+3OH-═Al(OH)3↓ |
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、a点所示溶液中:c(Na+)=c(CH3COOH)+c(CH3COO-) |
| B、b和c点所示溶液中:c(OH-)-c(H+)=c(Na+)-c(CH3COO-) |
| C、d点所示溶液中:c(Na+)>c(CH3COO-)>c(OH-)>c(H+) |
| D、滴定过程中可能出现:c(CH3COOH)>c(CH3COO-)>c(H+)>c(Na+)>c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、CaO(s) |
| B、CuO(s) |
| C、H2SO4(浓) |
| D、NaCl(s) |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com