
J、M、R、T是原子序数依次增大的短周期主族元素,J、R在周期表中的相对位置如下表。已知J元素最低负化合价的绝对值与其原子最外层电子数相等,M是地壳中含量最多的金属元素。

下列说法错误的是
A.J和氢组成的气态氢化物分子中可能只含有极性共价键
B.M单质能与氢氧化钠溶液反应,产生一种可燃性气体
C.R、T两元素的气态氢化物中,R的气态氢化物更稳定
D.J、M、R、T元素最高价氧化物对应的水化物中酸性最强的是HTO4
科目:高中化学 来源:2014-2015学年福建省高二上学期期中化学(文)试卷(解析版) 题型:选择题
3NO2十H2O==2HNO3十NO为工业上氨催化氧化法制硝酸的反应之一,该反应中NO2的作用是
A.只作氧化剂 B.作催化剂
C.既作氧化剂又作还原剂 D.作干燥剂
查看答案和解析>>
科目:高中化学 来源:2014-2015学年福建省高三第一次月考化学试卷(解析版) 题型:实验题
(14分)实验室需要0.80mol/LNaOH溶液475mL和0.40mol/L硫酸溶液500mL。根据这两种溶液的配置情况回答下列问题:
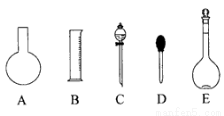
(1)如图所示的仪器中配制溶液肯定不需要的是 (填序号),配制上述溶液还需用到的玻璃仪器是 (填仪器名称)。
(2)下列操作中,容量瓶所不具备的功能有 (填序号。)
A.配制一定体积准确浓度的标准溶液
B.量取一定体积的液体
C.测量容量瓶规格以下的任意体积的液体
D.准确稀释某一浓度的溶液。
E.贮存溶液
F.用来加热溶解固体溶质
(3)根据计算得知,所需质量分数为98%、密度为1.84 g/cm3的浓硫酸的体为 mL(保留一位小数)。如果实验室有10mL、15mL、20mL、50mL量筒,应选用 mL量筒最好。
(4)根据计算用托盘天平称取NaOH的质量为 g。在实验中其他操作均正确,若定容时俯视视刻度线,则所得溶液浓度 0.8 mol/L(填“大于”、“等于”或“小于”,下同)。若定容时,有少许蒸馏水洒落在容量瓶外,则所得溶液浓度 0.8 mol/L。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年福建省高三第一次月考化学试卷(解析版) 题型:选择题
设NA为阿伏加德罗常数的数值,下列说法正确的是
A.常温下,23g NO2含有NA个氧原子
B.1 L 0.1 mol?L-1的氨水含有0.1NA个OH―
C.标准状况下,22.4 L CCl4含有NA 个CCl4分子
D.1 mol Fe2+与足量的H2O2溶液反应,转移2NA个电子
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东省济宁市高三上学期期中化学试卷(解析版) 题型:填空题
(8分)某一离子反应体系有反应物和产物共以下六种:MnO4-、H+、O2、H2O、H2O2、Mn2+,
已知该反应中的H2O2只发生如下过程: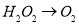
(1)该反应中的还原剂是 ,还原产物是________。
(2)KMnO4溶液随着酸性的增强氧化性不断增强,应选择_______(选填“稀硫酸”或“浓盐酸”)进行KMnO4溶液的酸化。
(3)假如反应转移了0.3mol电子,则产生的气体在标准状况下体积为________。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东省济宁市高三上学期期中化学试卷(解析版) 题型:选择题
在下列溶液中,能大量共存的离子组是
A.能使pH试纸显蓝色的溶液中:K+、Ba2+、H+、Br-
B.加入Al能放出H2的溶液中:K+、Na+、NO3-、Cl-
C.含有大量Fe3+的溶液中:SCN-、I-、K+、Br-
D.能使石蕊试液显红色的溶液中:K+、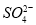 、S2-、
、S2-、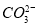
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河北省高三12月月考化学试卷(解析版) 题型:填空题
A、B、C、D、E五种短周期元素(A、B、C、D、E分别代表元素符号),它们的原子序数依次增大;A是元素周期表中原子半径最小的元素;B元素最高价氧化物对应的水化物与其氢化物反应生成一种盐X;D与A同主族,且与E同周期;E元素原子的最外层电子数是其次外层电子数的=3/4倍;C与E同主族。请回答下列问题:
(1)X的化学式为______
(2)元素的非金属性C______E(填“>”、“<”或“=”),下列各项中,能说明这一结论的事实有______(填序号)。
①氢化物H2E的酸性比H2C强
②氢化物H2C的热稳定性比H2E强
③氢化物H2E的水溶液放置在空气中会变浑浊
(3)将由BC和BC2组成的混合气体通入下图所示装置中,用来验证浓硝酸的氧化性比稀硝酸的氧化性强。

已知(ⅰ)浓硝酸能将气体BC氧化成BC2,而稀硝酸不能氧化BC。
(ⅱ)NaOH溶液与BC2反应的化学方程式为:
2NaOH+2BC2 NaBC2+NaBC + H2O
NaBC2+NaBC + H2O
NaOH溶液与BC气体不反应
a.装置①、②、③中盛放的药品依次是______、______、______。
b.通入混合气体之前,应先通入一段时间某另外一种气体,试推测先通入的该气体可以是______(填一种气体的化学式)。
c.能够说明实验已成功的现象是___________________________。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河北省高三12月月考化学试卷(解析版) 题型:选择题
向盐酸中加浓H2SO4时,会有白雾生成,不是导致产生该现象的原因是
A.浓H2SO4具有脱水性
B.浓H2SO4具有吸水性
C.盐酸具有挥发性
D.气态溶质的溶解度随度随温度的升高而降低
查看答案和解析>>
科目:高中化学 来源:2014-2015学年甘肃省高三11月月考化学试卷(解析版) 题型:实验题
(14分)氯化硫(S2Cl2)是一种黄红色液体,有刺激性、窒息性恶臭,熔点为-80℃,沸点137.1℃。在空气中强烈发烟,易与水发生水解反应。人们使用它作橡胶硫化剂,使橡胶硫化,改变生橡胶热发粘冷变硬的不良性能。在熔融的硫中通入氯气即可生成S2Cl2。下图是实验室用S和Cl2制备S2Cl2的装置(夹持装置、加热装置均已略去)。
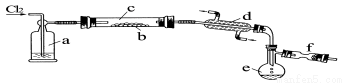
(1)已知S2Cl2分子结构与H2O2相似,请写出S2Cl2的电子式 。
(2)装置a中应放试剂为 ,其作用为 ;装置c为何水平放置 ;
(3)该实验的操作顺序应为 (用序号表示)。
①加热装置c ②通入Cl2 ③通冷凝水 ④停止通Cl2 ⑤停止加热装置c
(4)f装置中应放置的试剂为 ,其作用为 。
(5)已知S2Cl2水解时,只有一种元素的化合价发生了变化,且被氧化和被还原的该元素的物质的量之比为1:3,请写出该反应的化学方程式 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com