
【题目】如图所示,可逆反应:2A(g)+B(g)2C(g)△H<0的图象正确的是( )
A.
B.
C.
D.
【答案】A
【解析】解:A.△H<0为放热反应,温度高反应速率快,升高温度平衡逆向移动,则温度高时先达到平衡状态,且C%的含量低,故A正确;
B.该反应为气体体积减小的反应,增大压强平衡正向移动,则交叉点后正反应速率大于逆反应速率,故B错误;
C.该反应为放热反应,升高温度,平衡逆向移动,且正逆反应速率均增大,图中速率减小不符合,故C错误;
D.升高温度平衡逆向移动,则温度高时A的转化率小,图象不符,故D错误;
故选A.
【考点精析】解答此题的关键在于理解化学平衡状态本质及特征的相关知识,掌握化学平衡状态的特征:“等”即 V正=V逆>0;“动”即是动态平衡,平衡时反应仍在进行;“定”即反应混合物中各组分百分含量不变;“变”即条件改变,平衡被打破,并在新的条件下建立新的化学平衡;与途径无关,外界条件不变,可逆反应无论是从正反应开始,还是从逆反应开始,都可建立同一平衡状态(等效).


科目:高中化学 来源: 题型:
【题目】氨、硫、氯及其化合物对环境有着重要的影响,在化工生产和日常生活中的用途也十分广泛,如用做漂白剂、沉淀剂、农药、化肥等.
(1)以N2 和H2 为原料合成氢气的反应为:N2(g)+3H2(g)2NH3(g)△H=QkJ.mol﹣1 . 已知N﹣N 键键能为946kJ.mol﹣1 , H﹣H键键能为436kJ.mol ﹣1 , N﹣H键键能为391kJ.mol﹣1 , 则Q= .
(2)将体积均为560mL(标准状况下)的SO2 和Cl2 同时缓慢通水中,得到1.0L溶液,则溶液pH= .
(3)物质的量浓度相等的NH4HSO3溶液和NaHSO3溶液中,阴离子的电离程度较小的是(填化学式),原因是
(4)用惰性电极电解NaHSO3 溶液的装置如图所示,则I是(填化学式,下同),阳极区放出的混合气体的成分为 . 
(5)氨水是一种常见的沉淀剂.向1.0L2.0×10﹣4mol.L﹣1的MgCl2 溶液中通入 (不考虑溶液体积的变化),有白色沉淀生成.
①写出生成白色沉淀的离子方程式
②当反应中开始有白色沉淀出现时,通人的体积(标准状况)为 mL.(已知实验条件下NH3 . H2O的电离平衡常数为1.8×l0﹣5 , Ksp[Mg(OH)2]=1.8×10﹣11)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是( )
A.正丁烷的沸点比异丁烷的高
B.甲烷、苯、葡萄糖均不能使溴水或酸性高锰酸钾溶液褪色
C.羊毛、蚕丝、塑料、合成橡胶都性属于有机高分子材料
D.天然植物油没有恒定的熔沸点,常温下难溶于水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是( )
A.NH4+、Al3+、Cl﹣、HCO3﹣在溶液中能大量共存
B.H2O2的电子式是: ![]()
C.AlCl3溶液中加入过量的氨水:Al3++3NH3H2O═Al(OH)3↓+3NH4+
D.铁锈是化合物,可用Fe2O3nH2O(2<n<3)表示
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验误差分析错误的是( )
A.用润湿的pH试纸测稀碱溶液的pH,测定值偏小
B.用容量瓶配制溶液,定容时俯视刻度线,所配溶液浓度偏小
C.滴定前滴定管内无气泡,终点读数时有气泡,所测体积偏小
D.测定中和反应的反应热时,将碱缓慢倒入酸中,所测温度值偏小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮及其化合物在工农业生产、生活中有着重要作用.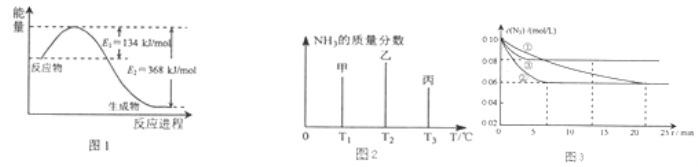
(1)图1是1molNO2和1mol CO反应生成CO2和NO过程中能量变化示意图,请写出NO2和CO反应的热化学方程式 .
(2)在固定容积的密闭容器中,进行如下化学反应:N2(g)+3H2(g)2NH3(g)△H=﹣92.4kJmol﹣1 用一定物质的量的N2和H2合成NH3 , 三个容器的反应温度分别为T1、T2、T3且恒定不变,在其它条件相同的情况下,实验测得反应均进行到t min时NH3的质量分数如图2所示:
此时甲、乙、丙三个容器中一定达到化学平衡状态的是容器,都达到平衡状态时,NH3的质量分数最高的是容器(填甲、乙、丙).
图3是实验室在三个不同条件的密闭容器中,分别加入浓度均为c(N2)=0.10mol/L,c(H2)=0.26mol/L进行反应时,N2的浓度随时间的变化如图①、②、③曲线所示.
Ⅰ该反应实验②平衡时H2的转化率为 .
Ⅱ据图3所示,②装置中有一个条件与①不同,请指出②相对①改变的条件 .
Ⅲ计算实验③的平衡常数为 .
(3)铜与一定浓度硝酸反应时方程式可表示为:Cu+HNO3一Cu(NO3)2+NO+NO2+H2O(方程式未配平).3.2g Cu被硝酸完全溶解后,如果得到的NO和NO2物质的量相同,则得到标准状况下NO体积为 L.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E、F六种短周期元素的简单离子都含有10个电子,且对应元素化合价与原子序数的关系如图所示。

(1)将A、E两种元素的元素符号填入下表中正确的位置上。________
族序数 周期 | IA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
一 | ||||||||
二 | ||||||||
三 | ||||||||
(2)A、B、C、D、E、F六种元素中非金属性最强的是____________(填元素符号),B、D两元素可以组成原子个数比为1:1的离子化合物,写出该离子化合物的电子式:______,A、B两元素对应的气态氢化物的稳定性强弱关系是________________(用化学式表示)。
(3)写出D、F两元素的最高价氧化物对应的水化物反应的离子方程式:________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组离子在给定条件下一定能大量共存的是( )
A.滴加甲基橙显红色的溶液中:Na+、K+、Cl﹣、ClO﹣
B.滴入KSCN显血红色的溶液中:Na+、Mg2+、SO42﹣、Br﹣
C.![]() =1.0×1012mol/L的溶液中:K+、Na+、NO3﹣、HCO3﹣
=1.0×1012mol/L的溶液中:K+、Na+、NO3﹣、HCO3﹣
D.由水电离的c(H+)=1.0×10﹣13mol/L的溶液中:NH4+、Fe2+、NO3﹣、SO42﹣
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com