
| A. | 常量组分分析 | B. | 微量组分分析 | C. | 痕量组分分析 | D. | 超痕量组分分析 |
分析 A.常量分析指的是被测试样的量m>0.1g或者V>10ml的分析,组分含量为1-100%;
B.微量分析一般指试样重量为0.1-10mg或体积为0.01-1ml或组分含量为0.01%~1%的化学分析;
C.痕量分析包括测定痕量元素在试样中的总浓度,和用探针技术测定痕量元素在试样中或试样表面的分布状况.一般分成3 个基本步骤:取样、样品预处理和测定,组分含量<0.01%;
D.组分含量为约0.0001%,为超痕量组分分析.
解答 解:依据分析可知某试样中被分析的组分在试样中的相对含量为0.08%,相对含量介于0.01%~1%的化学分析称为微量组分分析,
故选B.
点评 本题考查了分析化学中的常量分析、微量分析、痕量分析和超微量分析的区分和判断,注意知识的积累,题目难度不大.


 举一反三单元同步过关卷系列答案
举一反三单元同步过关卷系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
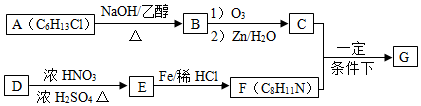
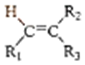 $→_{②Zn/H_{2}O}^{①O_{3}}$R1CHO+
$→_{②Zn/H_{2}O}^{①O_{3}}$R1CHO+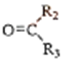
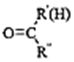 $\stackrel{一定条件}{→}$
$\stackrel{一定条件}{→}$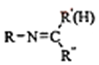 +H2O
+H2O .
. (写出其中一种的结构简式).
(写出其中一种的结构简式).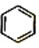 $\stackrel{一定条件1}{→}$H$\stackrel{反应条件2}{→}$I$→_{一定条件}^{C}$J$\stackrel{还原}{→}$
$\stackrel{一定条件1}{→}$H$\stackrel{反应条件2}{→}$I$→_{一定条件}^{C}$J$\stackrel{还原}{→}$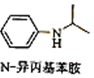
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铁粉表面的油污用热的纯碱溶液去油污效果更好 | |
| B. | 常温下,向水中加入少量固体硫酸氢钠,c(H+)增大,Kw不变 | |
| C. | 制备无水的AlCl3、FeCl3均不能采用将溶液在空气中直接蒸干的方法 | |
| D. | 室温下,向0.1mol•L-1的HF溶液中加入水溶液显碱性的物质,HF的电离程度一定增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 实验室制备氯气时用碱液吸收尾气:Cl2+OH-═Cl-+ClO-+H2O | |
| B. | 碳酸氢钠中滴加澄清石灰水:CO32-+Ca2+═CaCO3↓ | |
| C. | 大理石用盐酸溶解:CaCO3+2H+═Ca2++CO2↑+H2O | |
| D. | 腐蚀电路板的原理:Fe3++Cu═Fe2++Cu2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在H2O2+Cl2═2HCl+O2反应中,每生成32g氧气,则转移4NA个电子 | |
| B. | 100g质量分数为98%的浓硫酸中所含有的氧原子数为4NA | |
| C. | NA个H2分子与NA个D2O分子的质量比为1:9 | |
| D. | 标准状况下,5.6g乙烯和丙烯的混合气体中含C-H键的数目为0.8NA |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com