
原电池的电极名称不仅与电极材料的性质有关,也与电解质溶液有关,下列说法中不正确的是
A.由Al、Cu、稀H2SO4组成原电池,放电时SO42-向Al电极移动
B.由Mg、Al、NaOH溶液组成原电池,其负极反应式为:Al-3e-+4OH-=AlO2-+2H2O
C.由Fe、Cu、NaCl溶液组成原电池,其负极反应式为:Cu - 2e-= Cu2+
D.由Al、Cu、浓硝酸组成原电池作电源,用石墨电极来电解硝酸银溶液,当析出1 mol Ag时,消耗Cu电极32g
C
【解析】
试题分析:A.由Al、Cu、稀H2SO4组成原电池,Al作负极,Cu作正极,根据同种电荷相互排斥,异种电荷相互吸引,所以放电时SO42-向正电荷较多的负极Al电极移动,正确;B.由Mg、Al、NaOH溶液组成原电池,Al作负极。其负极反应式为:Al-3e-+4OH-=AlO2-+2H2O,正确;C.由Fe、Cu、NaCl溶液组成原电池,发生吸氧腐蚀,Fe活动性比Cu强,作负极,Cu作正极,其负极反应式为:Fe-2e-=Fe2+,错误;D.由Al、Cu、浓硝酸组成原电池,由于Al在浓硝酸中会发生钝化,所以Cu作负极,Al作正极,该原电池作电源,用石墨电极来电解硝酸银溶液,因为在整个闭合回路中电子转移数目相等。当析出1 mol Ag时,电子转移1mol,则消耗的Cu的质量为32 g,正确,选C。
考点:考查原电池的工作原理。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2014-2015学年山西省校高二上学期期中化学试卷(解析版) 题型:选择题
下列说法中正确的是
A.在25℃的纯水中,c(H+)=c(OH-)=10-7 mol/L,呈中性
B.溶液中若c(H+)>10-7 mol/L,则c(H+)>c(OH-),溶液显酸性
C.c(H+)越大,则pH值越大,溶液的碱性越强
D.pH值为0的溶液中c(H+) = 0 mol/L
查看答案和解析>>
科目:高中化学 来源:2015届江苏省高二上学期期中化学试卷(解析版) 题型:填空题
(12分)短周期主族元素A、B、C、D的原子序数依次增大,其中A、C同主族,B、C、D同周期,A原子的最外层电子数是次外层电子数的3倍,B是短周期元素中原子半径最大的主族元素。试回答下列问题:
(1)A的元素符号 ;B的元素名称 ;
(2)D的原子的电子式 ;C原子的电子排布式 。
(3)A、B、C三种元素形成的简单离子的半径由大到小的顺序是 。
(4)CA2与D元素的单质在水溶液中反应的化学方程式是 。
查看答案和解析>>
科目:高中化学 来源:2015届江苏省高二上学期期中化学试卷(解析版) 题型:选择题
下列关于氢原子电子云图的说法正确的是
A.通常用小黑点来表示电子的多少,黑点密度大,电子数目大。
B.黑点密度大,单位体积内电子出现的机会大。
C.通常用小黑点来表示电子绕核作高速圆周运动。
D.电子云图是对运动无规律性的描述。
查看答案和解析>>
科目:高中化学 来源:2014-2015河南省濮阳市高二上学期第三次质量检测化学试卷(解析版) 题型:填空题
(18分)依据氧化还原反应:2Ag+(aq)+Cu(s)===Cu2+(aq)+2Ag(s)设计的原电池,如图所示。
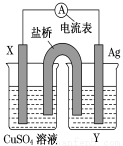
请回答下列问题:
(1)电极X的材料是________;电解质溶液Y是________溶液。(填名称)
(2)银电极为电池的________极,发生的电极反应为____________________________;X电极上发生的电极反应为____________________________。
(3)外电路中的电子是从________极流向______极(填电极材料)。外电路中每通过0.1 mol电子,银电极的质量理论上增加 g。
(4)原电池工作时,盐桥(装有琼脂-KCl的U型管)里的Cl-移向 电极。
查看答案和解析>>
科目:高中化学 来源:2014-2015河南省濮阳市高二上学期第三次质量检测化学试卷(解析版) 题型:选择题
在蒸发皿中加热蒸干下列物质的溶液,再灼烧(溶液低于400℃)可以得到原溶质固体的是
A.AlCl3 B.NaHCO3 C.MgSO4 D.KMnO4
查看答案和解析>>
科目:高中化学 来源:2014-2015河南省濮阳市高二上学期第三次质量检测化学试卷(解析版) 题型:选择题
将等质量的两份锌粉a、b分别加入过量的稀硫酸。同时向a中加入少量CuSO4溶液。图中产生H2的体积V L与时间t min的关系正确的是
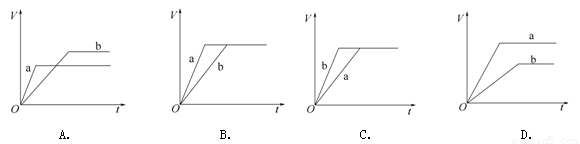
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河北省邢台市高三上学期第四次月考化学试卷(解析版) 题型:实验题
(10分).苯甲酸广泛应用于制药和化工行业,某同学尝试用甲苯的氧化反应制备苯甲酸,反应原理:
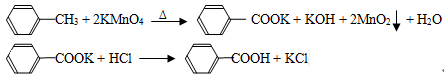
实验方法:一定量的甲苯和KMnO4溶液在100℃反应一段时间后停止反应,按如下流程分离出苯甲酸和回收未反应的甲苯。
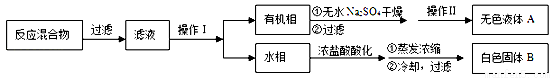
已知:苯甲酸分子量122,熔点122.4℃,在25℃和95℃时溶解度分别为0.3 g和6.9 g;纯净固体有机物都有固定熔点。
(1)操作Ⅰ为 ,操作Ⅱ为 。
(2)无色液体A是 ,定性检验A的试剂是 ,现象是 。
(3)测定白色固体B的熔点,发现其在115℃开始熔化,达到130℃时仍有少量不熔,该同学推测白色固体B是苯甲酸与KCl的混合物,设计了如下方案进行提纯和检验,实验结果表明推测正确。请在答题卡上完成表中内容。
序号 | 实验方案 | 实验现象 | 结论 |
① | 将白色固体B加入水中,加热溶 解, | 得到白色晶体和无色溶液 | ----------------- |
② | 取少量滤液于试管中, | 生成白色沉淀 | 滤液含Cl— |
③ | 干燥白色晶体, | 熔点为122.4℃ | 白色晶体是苯甲酸 |
(4)纯度测定:称取1.220g产品,配成100ml甲醇溶液,移取25.00ml溶液,滴定,消耗KOH的物质的量为2.40×10—3mol,产品中苯甲酸质量分数为 (保留二位有效数字)。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年福建省高三上学期期中考试化学试卷(解析版) 题型:选择题
下列五种有色溶液与SO2作用均能褪色,其实质相同的是
①品红溶液;②酸性KMnO4溶液;③溴水;④滴有酚酞的NaOH溶液;⑤含I2的淀粉溶液
A.①④ B.①②③ C.②③⑤ D.③④
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com