
| A. | 可用作荧光灯内壁保护层的氧化铝纳米材料属于胶体 | |
| B. | 淀粉、纤维素和油脂都是天然高分子化合物 | |
| C. | 古代的陶瓷、砖瓦、现代的玻璃、水泥等,都是硅酸盐产品 | |
| D. | 钢化玻璃、有机玻璃、防弹玻璃均属于硅酸盐材料 |
分析 A.胶体是分散质粒子介于1-100nm之间的分散系,属于混合物;
B.根据高分子化合物的定义判断;
C.陶瓷、玻璃、水泥主要成分都是硅酸盐;
D.有机玻璃的主要成分是有机物.
解答 解:A.胶体是分散质粒子介于1-100nm之间的分散系,属于混合物,而荧光灯内壁保护层的纳米氧化铝是纯净物,故不是胶体,故A错误;
B.高分子化合物的相对分子质量在10000以上,而油脂的相对分子质量较小,不是高分子化合物,故B错误;
C.古代的陶瓷、砖瓦、现代的玻璃、水泥等,都是硅酸盐产品,故C正确;
D.有机玻璃的主要成分是有机物,不是硅酸盐,故D错误;
故选:C.
点评 本题考查了化学知识在生产和生活中的运用,熟悉胶体、高分子化合物的概念,常见的硅酸盐产品是解题关键,题目难度不大.


 智能训练练测考系列答案
智能训练练测考系列答案科目:高中化学 来源: 题型:解答题
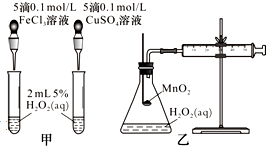 影响化学反应速率的因素很多,某课外兴趣小组用实验方法进行探究.
影响化学反应速率的因素很多,某课外兴趣小组用实验方法进行探究.| 序号 | 温度/℃ | 催化剂 | 现象 | 结论 |
| 1 | 40 | FeCl3溶液 | ||
| 2 | 20 | FeCl3溶液 | ||
| 3 | 20 | MnO2 | ||
| 4 | 20 | 无 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 蚊虫叮咬处涂抹肥皂水可止痛痒 | |
| B. | 金属钠、电石着火时,直接用高压水枪喷水扑灭 | |
| C. | 玛瑙饰品的主要成分与建筑材料砂子相同 | |
| D. | 家庭中洁厕灵与“84消毒液”不能同时使用 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 碳和氮是地球上含量丰富的两种元素,其氧化物的化学热力学、动力学研究有助于人类充分利用化石燃料,消除氧化物对环境的负面影响.
碳和氮是地球上含量丰富的两种元素,其氧化物的化学热力学、动力学研究有助于人类充分利用化石燃料,消除氧化物对环境的负面影响. CO2(g)+NO(g)△H=a-bkJ/mol或△H=-(b-a)kJ/mol;
CO2(g)+NO(g)△H=a-bkJ/mol或△H=-(b-a)kJ/mol;| 温度/℃ | n (C)/mol | n(CO2)/mol |
| T1 | 0.3 | |
| T2 | 0.75 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 不需要加热就能发生的反应一定是放热反应 | |
| B. | 弱电解质溶液的导电能力一定比强电解质溶液的弱 | |
| C. | SO2溶于水,其水溶液能导电,故SO2是电解质 | |
| D. | 蔗糖、碳酸钙和水分别属于非电解质、强电解质和弱电解质 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 元素 Y的单质与氢氧化钠溶液或盐酸反应均有氢气生成 | |
| B. | 元素 X与 W形成的共价化合物有很多种 | |
| C. | 元素 W、X的氯化物中,各原子均满足 8 电子的稳定结构 | |
| D. | 元素 Z 可与元素 X 形成共价化合物 XZ2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 (提示:
(提示: 可表示为
可表示为 )
)
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 ,G中的化学键有离子键、共价键,D跟G反应的化学方程式为2Na2O2+2CO2=2Na2CO3+O2.
,G中的化学键有离子键、共价键,D跟G反应的化学方程式为2Na2O2+2CO2=2Na2CO3+O2.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com