
| A£® | ¢Ł¢Ū¢Ü¢Ż¢ą | B£® | ¢Ū¢Ü¢Ż¢Ž¢ą | C£® | ¢Ś¢Ü¢Ż¢Ž¢ß | D£® | ¢Ł¢Ś¢Ü¢Ż¢ą |
·ÖĪö »Æѧ·“Ó¦øł¾ŻÄÜĮæ±ä»Æ·ÖĪŖĪüČČ·“Ó¦ŗĶ·ÅČČ·“Ó¦£¬³£¼ūµÄ·ÅČČ·“Ó¦ÓŠ£ŗĖłÓŠµÄĪļÖŹČ¼ÉÕ”¢ĖłÓŠ½šŹōÓėĖį·“Ó¦”¢½šŹōÓėĖ®·“Ó¦”¢ĖłÓŠÖŠŗĶ·“Ó¦”¢¾ų“󶹏ż»ÆŗĻ·“Ó¦ŗĶĀĮČČ·“Ó¦£»
³£¼ūµÄĪüČČ·“Ó¦ÓŠ£ŗ¾ų“óŹż·Ö½ā·“Ó¦”¢øö±šµÄ»ÆŗĻ·“Ó¦£ØČēCŗĶCO2£©”¢ÉŁŹż·Ö½ā”¢ÖĆ»»ŅŌ¼°Ä³Š©ø“·Ö½ā·“Ó¦£ØČēļ§ŃĪŗĶĒæ¼ī£©µČ£»
ĪļĄķ±ä»Æ¼Č²»ŹĒĪüČČ·“Ó¦Ņ²²»ŹĒ·ÅČČ·“Ó¦£®
½ā“š ½ā£ŗ¢Ł¼ÓČČKClO3ŗĶMnO2µÄ»ģŗĻĪļÖĘČ”O2ŹĒ·Ö½ā·“Ó¦£¬ŹōÓŚĪüČČ·“Ó¦£»
¢ŚĄÆÖņµÄČ¼ÉÕŹĒ·ÅČČ·“Ó¦£»
¢ŪĢ¼ŗĶ¶žŃõ»ÆĢ¼ŌŚøßĪĀĻĀ·“Ó¦ŹĒĪüČČ·“Ó¦£»
¢Ü½«ĒāŃõ»Æ±µ¾§ĢåŗĶĀČ»Æļ§¾§ĢåµÄ»ģŗĻĪļ·ÅČėĖ®ÖŠŹĒĪüČČ·“Ó¦£»
¢Ż½«Ģ¼ĖįÄĘ¾§ĢåŗĶĻõĖįļ§¾§Ģå»ģŗĻ¾łŌČ·ÅŌŚČÕ¹āĻĀ±©É¹£¬ŹĒĪüČČ·“Ó¦£»
¢Ž½«š¤ĶĮ”¢ŹÆ×Ó”¢Ė®»ģŗĻ¾łŌČ£¬ŹĒĪļĄķ±ä»Æ£¬¼Č²»ŹĒĪüČČ·“Ó¦Ņ²²»ŹĒ·ÅČČ·“Ó¦£»
¢ß½«ÉśŹÆ»Ņµ¹Čėŗ£Ė®ÖŠ£¬Ńõ»ÆøĘŗĶĖ®·“Ӧɜ³ÉĒāŃõ»ÆøĘ£¬ŹĒ·ÅČČ·“Ó¦£»
¢ąģŃÉÕŹÆ»ŅŹÆŹĒĪüČČ·“Ó¦£»
¹ŹŃ”A£®
µćĘĄ ±¾Ģāæ¼²éĪüČČ·“Ó¦£¬×„ה֊ѧ»Æѧ֊³£¼ūµÄĪüČČ»ņ·ÅČȵķ“Ó¦ŹĒ½āĢāµÄ¹Ų¼ü£¬¶ŌÓŚĢŲŹā¹ż³ĢÖŠµÄČČĮæ±ä»ÆµÄŅŖŹģĮ·¼ĒŅ䥓½ā“š“ĖĄąĻ°Ģā£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
| ĪļÖŹ | Cu£ØOH£©2 | Fe£ØOH£©3 | CuCl | CuI |
| Ksp | 2.2”Į10-20 | 2.6”Į10-39 | 1.7”Į10-7 | 1.3”Į10-12 |

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ²ŻĖįÓėĖįŠŌøßĆĢĖį¼ŲČÜŅŗ·“Ó¦£ŗ2MnO4-+5H2C2O4+6H+ØT2Mn2++10CO2”ü+8H2O | |
| B£® | Įņ“śĮņĖįÄĘÓėĮņĖįµÄĄė×Ó·½³ĢŹ½£ŗS2O32-+2H+ØTSO2”ü+S”ż+H2O | |
| C£® | KIČÜŅŗÖŠµĪ¼ÓĻ”ĮņĖį£¬³ØæŚ·ÅÖĆ£ŗ2H++2I-+O2ØTI2+2H2O | |
| D£® | K2Cr2O7µÄČÜŅŗÖŠ“ęŌŚµÄĘ½ŗāĢåĻµ£ŗCr2O72-+H2O?2CrO42-+2H+ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
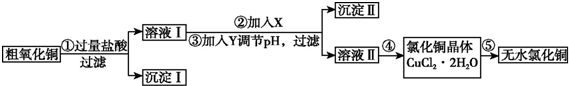
| ĒāŃõ»ÆĪļæŖŹ¼³ĮµķŹ±µÄpH | ĒāŃõ»ÆĪļ³ĮµķĶźČ«Ź±µÄpH | |
| Fe3+ | 1.9 | 3.2 |
| Fe2+ | 7.0 | 9.0 |
| Cu2+ | 4.7 | 6.7 |
| Ģį¹©µÄŹŌ¼Į£ŗa£®NaOH””””””b£®H2O2””””””c£®Na2CO3””””d£®CuO | ||
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
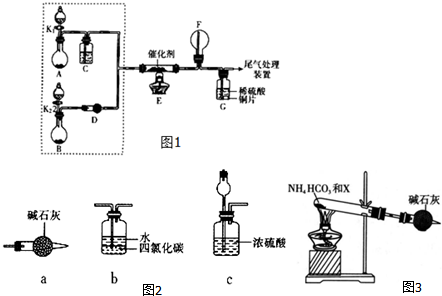
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
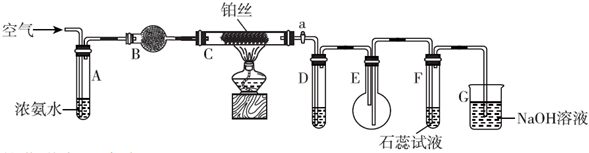
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
 ijŹµŃ銔×é¶Ō֊ѧæĪ±¾ÖŠæÉÉś³ÉĒāĘųµÄ·“Ó¦½ųŠŠĮĖŃŠ¾æ£¬×ܽį³öČżøöæÉŅŌÉś³ÉH2µÄ·“Ó¦£ŗ¢ŁZn+ŃĪĖį£»¢ŚNa+Ė®£»¢ŪAl+NaOHČÜŅŗ£®Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ
ijŹµŃ銔×é¶Ō֊ѧæĪ±¾ÖŠæÉÉś³ÉĒāĘųµÄ·“Ó¦½ųŠŠĮĖŃŠ¾æ£¬×ܽį³öČżøöæÉŅŌÉś³ÉH2µÄ·“Ó¦£ŗ¢ŁZn+ŃĪĖį£»¢ŚNa+Ė®£»¢ŪAl+NaOHČÜŅŗ£®Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ·Ö×Ó¾§ĢåÖŠŅ»¶Øŗ¬ÓŠ·Ö×Ó¼ä×÷ÓĆĮ¦£¬µ«²»Ņ»¶Øŗ¬ÓŠ¹²¼Ū¼ü | |
| B£® | Ąė×Ó¾§ĢåÖŠŅ»¶Øŗ¬ÓŠĄė×Ó¼ü£¬µ«²»Ņ»¶Øŗ¬ÓŠ¹²¼Ū¼ü | |
| C£® | Ō×Ó¾§ĢåÖŠŅ»¶Øŗ¬ÓŠ¹²¼Ū¼ü£¬Ó²¶Č“ó£¬ČŪ·Šµćøß | |
| D£® | Ō×Ó¾§Ģ嶼²»µ¼µē |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 46 | B£® | 34 | C£® | 30 | D£® | 60 |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com