
全钒液流电池是一种活性物质呈循环流动液态的电池,目前钒电池技术已经趋近成熟。下图是钒电池基本工作原理示意图:

请回答下列问题:
(1)硫酸在电池技术和实验室中具有广泛的应用,在传统的铜锌原电池中,硫酸是_________,实验室中配制硫酸亚铁时需要加入少量硫酸,硫酸的作用是__________。
(2)钒电池是以溶解于一定浓度硫酸溶液中的不同价态的钒离子(V2+、V3+、VO2+、VO )为正极和负极电极反应的活性物质,电池总反应为VO2++V3++H2O
)为正极和负极电极反应的活性物质,电池总反应为VO2++V3++H2O V2++VO
V2++VO +2H+。放电时的正极反应式为____________________________________________,
+2H+。放电时的正极反应式为____________________________________________,
充电时的阴极反应式为_________________________________________________。
放电过程中,电解液的pH________(填“升高”、“降低”或“不变”)。
(3)钒电池基本工作原理示意图中“正极电解液”可能是________(填字母序号)。
a.VO 、VO2+混合液 b.V3+、V2+混合液
、VO2+混合液 b.V3+、V2+混合液
c.VO 溶液 d.VO2+溶液
溶液 d.VO2+溶液
e.V3+溶液 f.V2+溶液
(4)能够通过钒电池基本工作原理示意图中“隔膜”的离子是______________________
__________________________________________________。
答 案 (1)电解质溶液 抑制硫酸亚铁的水解 (2)VO
案 (1)电解质溶液 抑制硫酸亚铁的水解 (2)VO +2H++e-===VO2++H2O V3++e-===V2+ 升高 (3)acd (4)H+
+2H++e-===VO2++H2O V3++e-===V2+ 升高 (3)acd (4)H+
解析 (1)传统的铜锌原电池中,锌与酸反应生成氢气,故硫酸为电解质溶液;硫酸亚铁容易水解,且水解显酸性,加入少量硫酸,可以抑制其水解变质。
(2)正极反应是还原反应,由电池总反应可知放电时的正极反应为VO +2H++e-===
+2H++e-===
VO2++H2O;充电时,阴极反应为还原反应,故为V3+得电子生成V2+的反应。
(3)充电时阳极反应式为VO2++H2O-e-===VO +2H+,故充电完毕的正极电解液为VO
+2H+,故充电完毕的正极电解液为VO 溶液,而放电完毕的正极电解液为VO2+溶液,故正极电解液可能是选项a、c、d。
溶液,而放电完毕的正极电解液为VO2+溶液,故正极电解液可能是选项a、c、d。
(4)充电和放电过程中,正极电解液与负极电解液不能混合,起平衡电荷作用的是加入的酸,故H+可以通过隔膜。


 每课必练系列答案
每课必练系列答案科目:高中化学 来源: 题型:
已知F为高分子化合物: 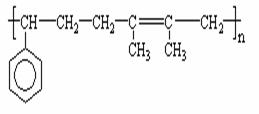 。 C分子结构中只含有一种氢。
。 C分子结构中只含有一种氢。
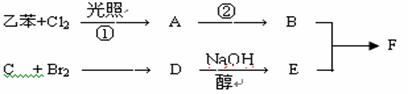
(1)写出下列物质结构简式
B: C: E:
(2)判断①反应类型:
(3)写出②反应进行所需条件:
(4)写出C7H8O所有含苯环结构的同分异构体: ——————————————
查看答案和解析>>
科目:高中化学 来源: 题型:
某航空站安装了一台燃料电池,该电池可同时提供电和水蒸气。所用燃料为氢气,电解质为熔融的碳酸钾。已知该电池的总反应为2H2+O2===2H2O,正极反应为O2+2CO2+4e-===2CO ,则下列推断正确的是 ( )
,则下列推断正确的是 ( )
A.负极反应为H2+2OH--2e-===2H2O
B.该电池可在常温或高温时进行工作,对环境具有较强的适应性
C.该电池供应2 mol水蒸气,同时转移2 mol电子
D.放电时负极有CO2生成
查看答案和解析>>
科目:高中化学 来源: 题型:
实验发现,298 K时,在FeCl3酸性溶液中加少量锌粒后,Fe3+立即被还原成Fe2+。某夏令营兴趣小组根据该实验事实设计了如图所示原电池装置。下列有关说法正确的是
( )

A.该原电池的正极反应是Zn-2e-===Zn2+
B.左烧杯中溶液的血红色逐渐褪去
C.该电池铂电极上有气泡出现
D.该电池总反应为3Zn+2Fe3+===2Fe+3Zn2+
查看答案和解析>>
科目:高中化学 来源: 题型:
下列反应既属于氧化还原反应,又属于吸热反应的是
A.铝片和稀盐酸反应 B.Ba(OH)2·8H2O与NH4Cl的反应
C.甲烷在氧气中的燃烧 D.灼热的碳与二氧化碳的反应
查看答案和解析>>
科目:高中化学 来源: 题型:
在密闭容器中进行的可逆反应X2(g)+Y2(g) 2Z (g),已知X2、Y2、Z的起始浓度分别为0.1mol/L、0.2mol/L、0.2mol/L,在一定条件下,当反应达到平衡时,Y2物质的浓度可能是
2Z (g),已知X2、Y2、Z的起始浓度分别为0.1mol/L、0.2mol/L、0.2mol/L,在一定条件下,当反应达到平衡时,Y2物质的浓度可能是
A. 0.35mol/L B. 0.2mol/L C. 0.4mol/L D. 0.3mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
下列化学用语不能正确解释相关事实的是
A.碱性氢氧燃料电池的正极反应:H2 - 2e- + 2OH-=== 2H2O
B.用电子式表示NaCl的形成过程:
C.向含有Hg2+的废水中加入Na2S可除去Hg2+:Hg2+ + S2- === HgS↓
D.汽车尾气系统的催化转化器可降低NO等的排放:2CO + 2NO 2CO2 +N2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com