
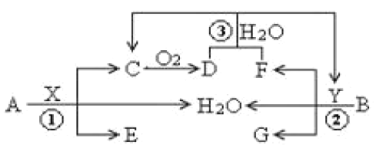
����Ŀ����֪���ֳ�������A(�ؿ��к����ڶ��Ľ���)��B(��ɫ����)�ֱ���������X��Y������Ӧ����ת����ϵ��ͼ��ʾ������DΪ����ɫ���塣
�ش��������⣺
��1����Ӧ�۵����ӷ�Ӧ����ʽΪ___��
��2��6.4gB�����X��Һ(8mol /L��60mL)��ַ�Ӧ�����ɵĻ�ԭ������C��D����Ӧ����Һ������XΪn mol ����ʱ��Һ������X�������ӵ����ʵ���Ϊ___mol��
��3��������A��Y��ϡ��Һ�ܷ�����Ӧ������W�����ڹ���W��ת����ϵ��ͼ��ʾ(����������ȥ)������N�Ǻ���ɫ�Ļ����

��M�����ֻ�������ɣ����к��Уƣ�����ͨ��BaCl2��Һ��ʵ��������___��
��������ӦI�õ�16 g����Σ�����������Mǡ�ñ�0.3L1mol��L��1 NaOH��Һ��ȫ���յ���Һ1����Ӧ���з�����Ӧ�����ӷ���ʽ��____��
���𰸡�SO2+NO2 +H2O=2H++SO42-+NO n+0.2 ������ɫ���� 2Fe3++HSO3-+H2O=2Fe2++SO42-+3H+
��������
��������AΪ�ؿ��к����ڶ��Ľ�����ȷ��ΪFe��BΪ��ɫ����ȷ��ΪCu������ DΪ����ɫ���壬ȷ��DΪNO2��CΪNO��XΪHNO3��BΪCu��ͭ������Ũ���ᷴӦ��������ͭ�����������ˮ�����ɵĶ��������л�ԭ�ԣ�������NO2��Ӧ������������ᣬȷ��BΪCu��YΪ���ᣬFΪSO2��GΪCuSO4����3��A��Fe����Y�����ᣩ��ϡ��Һ��Ӧ��������������������ȷ��WΪFeSO4��2FeSO4![]() Fe2O3+SO2��+SO3��������MΪSO2��SO3�Ļ���M��NaOH��Ӧ�����κ�ˮ��NΪFe2O3����ϡ���ᷴӦ������������ˮ��Fe3+���������Ժ�+4����Ԫ�ؾ��л�ԭ�ԣ����Է���������ԭ��Ӧ���������������ݴ˷�����
Fe2O3+SO2��+SO3��������MΪSO2��SO3�Ļ���M��NaOH��Ӧ�����κ�ˮ��NΪFe2O3����ϡ���ᷴӦ������������ˮ��Fe3+���������Ժ�+4����Ԫ�ؾ��л�ԭ�ԣ����Է���������ԭ��Ӧ���������������ݴ˷�����
��1���������Ϸ�����֪����Ӧ��ΪSO2��NO2��ˮ�ķ�Ӧ�����ݵ�ʧ��������Ⱥ�ԭ���غ���ƽ�������ӷ�Ӧ����ʽΪSO2+NO2 +H2O=2H++SO42-+NO��
�𰸣�SO2+NO2 +H2O=2H++SO42-+NO
��2��6.4gB�����X��Һ(HNO3)��ַ�Ӧ�����ɵĻ�ԭ������NO2��NO����Ӧ����Һ������HNO3Ϊn mol ����Һ������N![]() �����ʵ���Ϊ��n��N
�����ʵ���Ϊ��n��N![]() ��=n��Cu2+����2+n=
��=n��Cu2+����2+n=![]() +n= n+0.2mol��
+n= n+0.2mol��
�𰸣�n+0.2
��3���ٽ��ͣ�SO2��SO3��ͨ��BaCl2��Һ��������ӦSO3+H2O+BaCl2=BaSO4��+2HCl���а�ɫ�������ɣ�
�𰸣�������ɫ����
�ڷ�Ӧ��2FeSO4![]() Fe2O3+ SO2��+ SO3������Ӧ��Fe2O3+3H2SO4=Fe2(SO4)3+3H2O��
Fe2O3+ SO2��+ SO3������Ӧ��Fe2O3+3H2SO4=Fe2(SO4)3+3H2O��
���ݹ���M��Fe2O3�����������SO2��SO3�����ʵ�����
2FeSO4![]() Fe2O3+ SO2��+ SO3��
Fe2O3+ SO2��+ SO3��
160g 1mol 1mol
1.6g 0.01mol 0.01mol
��Ӧ�� SO3 + 2NaOH=Na2SO4+H2O
1mol 2mol 1mol
0.01mol 0.02mol 0.01mol
SO2+ NaOH = NaHSO3
1mol 1mol 1mol
0.01mol 0.01mol 0.01mol
��Һ1ΪNa2SO4��NaHSO3�Ļ���
��Ӧ�������������������ԣ����������ƾ��л�ԭ�ԣ����ݵ�ʧ��������Ⱥ�ԭ���غ�ó����ӷ���ʽ2Fe3++HSO3-+H2O=2Fe2++SO42-+3H+��
�𰸣�2Fe3++HSO3-+H2O=2Fe2++SO42-+3H+



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ��������ܱ������У��������»�ѧ��Ӧ��CO2(g)��H2(g)![]() CO(g)��H2O(g)����H=a kJ��mol��1�仯ѧƽ�ⳣ��K���¶�t�Ĺ�ϵ���±���
CO(g)��H2O(g)����H=a kJ��mol��1�仯ѧƽ�ⳣ��K���¶�t�Ĺ�ϵ���±���
t/�� | 700 | 800 | 830 | 1 000 | 1 200 |
K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
����˵������ȷ����(����)
A.�÷�Ӧ������ӦΪ���ȷ�Ӧ����a<0
B.��ƽ��Ũ�ȷ���c(CO2)��c(H2)=c(CO)��c(H2O)ʱ���¶�Ϊ830 ��
C.��������������ʱ������С������������������ڸ÷�Ӧƽ�������ƶ�
D.��v��(H2)=v��(H2O)ʱ�÷�Ӧ�ﵽ��ѧƽ��״̬
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijѧ��ͨ����ͼ��ʾʵ��װ�ý��е绯ѧʵ�顣ʵ��������£��ٱպ�S1����S2������20s���ڴ�S1���պ�S2���۲���������˵������ȷ����
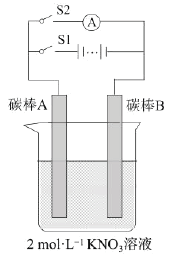
A.������ʱ�缫AΪ����������������Ӧ
B.������ʱ�缫BΪ������������B��Ǩ��
C.������ʱΪ���أ�������ʱΪԭ���
D.ʵ��������������Һ��Ũ�ȱ��ֲ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijδ֪��ҺX�п��ܺ���Mg2����Cu2����Fe3����Fe2����SO42����Cl���еļ��֣���������ʵ�飺
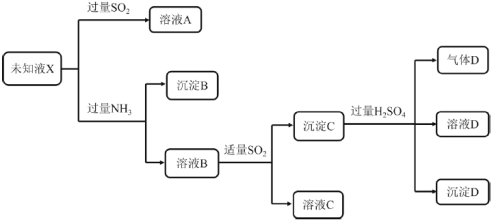
��֪��Cu2SO3Ϊ��ɫ���壬������ˮ��������ϡ���ᡣ����˵����ȷ����
A.δ֪ҺX��һ������Cu2����Fe3�������ܺ���Mg2��
B.��ҺB�к��д�����Cu2��
C.ȡ����B�������ܽ⣬�ټ���KSCN��Һ������Ѫ��ɫ��˵����ҺX��һ������Fe3��
D.����C��ϡ���ᷢ����������ԭ��Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ˮ�õ���ˮ����������ˮ�õ���ˮ�����й������Ƶİ�ˮ����ˮ����������ȷ���� (����)
A.����ˮ�����ǻ�����Һ�к��е�����������Ŀ��ͬ
B.����ˮ���ж����ڿ��淴Ӧ
C.����ˮ�����д̼�����ζ������Ư���л�ɫ��
D.����ˮ������ʱ��Ͼú���Ϊ��ͬ��ԭ��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���Ҷ��ᣬ�ֳƲ��ᣬͨ���ڿ������ױ����������ʡ��������ӽᾧˮ��H2C2O4��2H2O��ȴ���ڿ������ȶ����ڡ��ڷ�����ѧ�г���H2C2O4��2H2O��KMnO4�ĵζ��������й���H2C2O4��˵����ȷ����
A�������Ƕ�Ԫ���ᣬ����뷽��ʽΪH2C2O4![]() 2H++C2O
2H++C2O![]()
B������ζ�KMnO4�����к͵ζ�������ʯ����ָʾ��
C���Ҷ����ͨ����ϩ�����ӳɡ�ˮ�⡢�����������Ƶ�
D����ŨH2SO4�μӵ��Ҷ�����ʹ֮��ˮ�ֽ⣬�ֽ������CO2��H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��2019��ŵ������ѧ��������Լ��������˹�����ŵ��ɷ�˹̹������͢��ķ�ͼ�Ұ�ã���λ��ѧ�ҵĻ�������Ϊ﮵�صķ�չ������Խ���ס���ͼ���ҹ�һ�����Ʊ�����﮵��·�������ר��װ��ͼ������˵������ȷ����
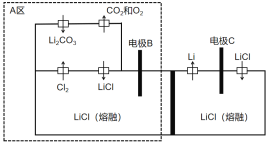
A.�缫B�ĵ��Ʊȵ缫C��
B.�����ϸ�װ�ò���Ҫ��������LiCl
C.�缫B�������Ӻ�̼������ӷŵ�
D.A����������̼��﮶��豸�ĸ�ʴ�Ҽ����˻�����Ⱦ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪п��Ũ���ᷴӦ����SO2����ϡ���ᷴӦ����H2��32.5�˵�п��50 mL 18.4 mol/LŨ�����ַ�Ӧ��п��ȫ�ܽ⣬ͬʱ�ռ�����״���µ�����VL������Ӧ�����Һϡ�͵�500mL�������Һ�������ӵ�Ũ��Ϊ0.08 mol/L��
(1)��Ӧ���������ĵ�H2SO4�����ʵ�����________��
(2)����ijɷ���______��VΪ______��
(3)��Ӧ������ת�Ƶĵ��ӵ����ʵ�����________��
(4)��ȡ��ͬŨ���ᣬ�����иļ����ۣ�������a�����ۣ�ͬʱ���ȣ��������ݾ�ͬ�ϣ���a=_____��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���±��������Ԫ�����ڱ���һ����Ԫ�ء�
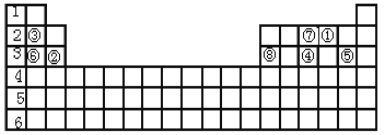
�����ϱ��ش��������⡣
��1��Ԫ�آٵ�ԭ��������____����Ԫ�آٹ�����ԭ�ӵ��ʵķ���������____��
��2��Ԫ�آ������ȣ�____Ԫ�ص�ԭ�Ӱ뾶�ϴ�____Ԫ�ص��⻯����ȶ�����Ԫ�ط�����д����
��3��Ԫ�آ������ȣ�����������Ӧˮ������Խϴ����________�����Ļ�ѧʽ����
��4��Ԫ�آں͢�������ﳣ�����ͻ���ϡ�Ԫ�آڵ�������Ļ�ѧʽ��______��Ԫ�آ�������������ռ���Һ��Ӧ�Ļ�ѧ����ʽ��____________��
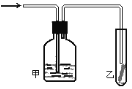
��5����ͼ������ʪ����Ԫ�آݹ��ɵĵ���ͨ����װ�ú���ͨ�����и����ɫ��������װ�ã���ɫ��������ɫ�����װ������ʢ�Լ�������______��
a��ϡ���� b��Ũ���� c��ˮ d������ʳ��ˮ
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com