
����Ŀ����ҵ��ˮ�г�����һ������Cr2O72����CrO42�������ǻ�����༰��̬ϵͳ�����ܴ���˺���������д��������õĴ������������֡�
����1����ԭ������
�÷��Ĺ�������Ϊ
![]()
���е���������ƽ�⣺2CrO42������ɫ��+2H+![]() Cr2O72������ɫ��+H2O
Cr2O72������ɫ��+H2O
��1����ƽ����ϵ��pH=2������Һ�� ɫ.
��2����˵����������Ӧ��ƽ��״̬���� ��
a��Cr2O72����CrO42����Ũ����ͬ b��2v (Cr2O72��) ="v" (CrO42��) c����Һ����ɫ����
��3���������У���ԭ1mol Cr2O72�����ӣ���Ҫ________mol��FeSO4��7H2O��
( 4 ) ���������ɵ�Cr(OH)3����Һ�д������³����ܽ�ƽ�⣺
Cr(OH)3(s)![]() Cr3+(aq)+3OH��(aq)
Cr3+(aq)+3OH��(aq)
�����£�Cr(OH)3���ܶȻ�Ksp��c(Cr3+)��c3(OH��)��10-32��Ҫʹc(Cr3+)����10-5mol/L����Һ��pHӦ���� ��
����2����ⷨ
�÷���Fe���缫��⺬Cr2O72�������Է�ˮ�����ŵ����У�������������ҺpH���ߣ�����Cr(OH)3������
��5����Fe���缫��ԭ��Ϊ ��
��6��������������ҺpH���ߵ�ԭ���ǣ��õ缫��Ӧ���ͣ� ��
��Һ��ͬʱ���ɵij������� ��
���𰸡���1���ȣ�2��c��3��6��4��5��5��������ӦΪFe��2e����Fe2+���ṩ��ԭ��Fe2+
��6��2H++2e����H2�� Fe(OH)3
����������1����ƽ����ϵ��pH=2��2CrO42������ɫ��+2H+![]() Cr2O72������ɫ��+H2O��ƽ�����ƣ��ʳ�ɫ��2����˵����������Ӧ��ƽ��״̬������Һ����ɫ���䣬��Һ�ĸ���Ӧ�����Ũ�Ȳ��䣬ѡc��3���ɵ�ʧ�����غ�ã�1mol Cr2O72�D��6�ۣ�Ҫ6molFe2����4��Ksp��c(Cr3��)��c3(OH��)��10-32��c3(OH��)= 10-32/10-5=10-27��c(OH��)= 10-9mol��L��1,pH= 5��5��������ӦΪFe��2e����Fe2�����ṩ��ԭ��Fe2��;�����������缫��6��������������ҺpH���ߵ�ԭ����2H��+2e����H2����ˮ����ƽ�ⱻ�ƻ�������OH�D�����ȣ�ʹCr(OH)3��Fe(OH)3��������ȥ��
Cr2O72������ɫ��+H2O��ƽ�����ƣ��ʳ�ɫ��2����˵����������Ӧ��ƽ��״̬������Һ����ɫ���䣬��Һ�ĸ���Ӧ�����Ũ�Ȳ��䣬ѡc��3���ɵ�ʧ�����غ�ã�1mol Cr2O72�D��6�ۣ�Ҫ6molFe2����4��Ksp��c(Cr3��)��c3(OH��)��10-32��c3(OH��)= 10-32/10-5=10-27��c(OH��)= 10-9mol��L��1,pH= 5��5��������ӦΪFe��2e����Fe2�����ṩ��ԭ��Fe2��;�����������缫��6��������������ҺpH���ߵ�ԭ����2H��+2e����H2����ˮ����ƽ�ⱻ�ƻ�������OH�D�����ȣ�ʹCr(OH)3��Fe(OH)3��������ȥ��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������йؾ���������У�������ǣ� ��
A. ���Ӿ�����һ���������Ӽ�B. ԭ�Ӿ����У�ֻ���ڹ��ۼ�
C. ���ɷ��Ӿ���������в����ڹ��ۼ�D. ϡ�������ԭ�����γɷ��Ӿ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Ҫ����գ�
(1)��S2��Fe2+��Fe3+��Mg2+��S��I��H+�У�ֻ�������Ե���____________��ֻ�л�ԭ�Ե���____________���������������л�ԭ�Ե���________��
(2)ijͬѧд������������ѧ����ʽ(δ��ƽ)��
��NO+HNO3��N2O3+H2O ��NH3+NO��HNO2+H2O ��N2O4+H2O��HNO3+HNO2
��������Ϊһ��������ʵ�ֵ���____________��
(3)��������������ԭ��Ӧ�У���������ǿ��������______________��
��2FeCl3+2KI![]() 2FeCl2+2KCl+I2
2FeCl2+2KCl+I2
��2FeCl2+Cl2![]() 2FeCl3
2FeCl3
��2KMnO4+16HCl(Ũ)![]() 2KCl+2MnCl2+5Cl2��+8H2O
2KCl+2MnCl2+5Cl2��+8H2O
��������Cl��I���棬Ϊ������I��Cl�����������������⣬��Ӧ��������Ӧ�е�__________����������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ϊ�˽�����K2SO4��MgSO4��KNO3�����ᴿ�����Ƶô�����KNO3��Һ��ijͬѧ�������ʵ�鷽����
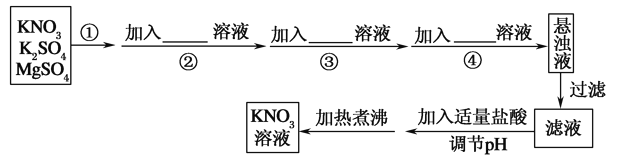
(1)������Ϊ________��
(2)����������������Լ������ֱ�Ϊ________��
(3)����ж�![]() �ѳ���������ʵ�����________________________��
�ѳ���������ʵ�����________________________��
(4)ʵ������в����Ķ�γ���________(���Ҫ������Ҫ��)��ι��ˣ�������_____________________��
(5)��ͬѧ��Ƶ�ʵ�鷽��________(���������������)��������____________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ij��ѧ�о���ѧϰС���ij��ɫˮ���ɷֵļ�����̣���֪��ˮ����ֻ���ܺ��� K+��Fe3+��Cu2+��Ag+��Ca2+��CO32-��SO42-��Cl-�е����������ӣ���С��ͬѧȡ 100 mL ˮ������ʵ�飺����Ʒ���ȵμ��Ȼ�����Һ���ٵμ� 1 mol��L-1 ���ᣬʵ������г��������ı仯��ͼ��ʾ������˵����ȷ����
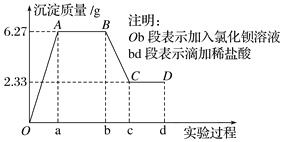
A. ˮ����һ��������Fe3+��Cu2+�����ܴ���Ag+
B. ˮ����һ������CO32-��SO42-��Cl-
C. BC����������ʾ�����ӷ���ʽΪCO32-��2H+=H2O��CO2��
D. ˮ����һ������K������c(K��)��0.6mol��L-1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����и�ѡ���л�����Ŀ�������ʽΪC4H7O2Cl������̼�����Ʒ�Ӧ����������л�����Ŀ��ͬ����
A. �ױ������ϵ�������ԭ�ӱ���ԭ��ȡ�� B. 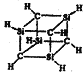 �Ķ��ȴ���
�Ķ��ȴ���
C. ����ʽΪC5H10 ��ϩ�� D. ����飨![]() ���Ķ��ȴ���
���Ķ��ȴ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һС������Ƴ�ʱ�����ڿ����У�����������������Щ������ֵ��Ⱥ�˳���ǣ� ��
�ٱ�ɰ�ɫ��ĩ �ڱ䰵 �۱�ɰ�ɫ���� �ܱ�����Һ������
A. �٢ڢۢ�B. �ڢۢܢ�C. �ڢۢ٢�D. �ۢڢܢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������ʹʪ��ĺ�ɫʯ����ֽ��������
A. C12 B. NO2 C. HCl D. NH3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ����Ƭ����500mL1mol/L CuSO4��Һ�У���Ӧһ��ʱ���ȡ����Ƭ��С��ϴ��������������Ƭ����0.8�磬��Ӧ����Һ��CuSO4�����ʵ���Ũ���ǣ���Ӧǰ����Һ��������䣩
A. 0.9mol/L B. 0.85mol/L C. 0.8mol/L D. 0.75mol/L
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com