
分析 (1)根据反应方程式Zn+H2SO4═ZnSO4+H2↑ 分析锌和硫酸的量的相对大小,根据计算锌的物质的量为0.12mol,硫酸的物质的量为0.1mol,可知锌过量,再根据反应方程式可计算出反应消耗的锌的质量进而可以推出剩余锌的质量以及生成氢气的体积;
(2)根据反应生成产物的物质的量以及溶液的体积可以推算出溶质的物质的量浓度.
解答 解:(1)设跟硫酸反应的锌的质量为x,反应后生成氢气的体积为y
Zn+H2SO4═ZnSO4+H2↑
65g 1mol 22.4L
x 0.1L×1mol/L y
$x=\frac{0.1mol×65g}{1mol}=6.5g$(1分)
锌有剩余;
剩余锌的质量为:7.8g-6.5g=1.3g
H2的体积$y=\frac{22.4L×0.1mol}{1mol}=2.24L$(1分)
(2)溶液的物质的量浓度为:$\frac{0.1mol}{0.25L}=0.4mol/L$(1分)
答:(1)锌有剩余;锌剩余的质量为1.3g;在标准状况下生成氢气的体积是2.24L;
(2)溶液中溶质的物质的量浓度为0.4mol/L.
点评 本题考查根据方程式的有关计算,比较基础,注意基础知识的理解掌握.


 小学能力测试卷系列答案
小学能力测试卷系列答案科目:高中化学 来源:2017届河南省高三上第二次月考化学试卷(解析版) 题型:选择题
向含有a mol FeBr2的溶液中通入x mol Cl2。下列各项为通Cl2过程中溶液内发生反应的离子方程式,其中不正确的是
A.x=0.4a,2Fe2++Cl2=2Fe3++2Cl-
B.x=0.6a,4Fe2++2Br-+3Cl2=Br2+4Fe3++6Cl-
C.x=a,2Fe2++2Br-+2Cl2=Br2+2Fe3++4Cl-
D.x=1.5a,2Fe2++4Br-+3Cl2=2Br2+2Fe3++6Cl-
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 金属钠在氯气中燃烧,有白雾生成 | |
| B. | 铜在氯气中燃烧,生成蓝色的氯化铜颗粒 | |
| C. | 红热的铁丝在氧气中剧烈燃烧,火星四射,生成黑色固体 | |
| D. | 氢气在氯气中燃烧产生大量的白烟 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 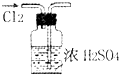 干燥Cl2 | B. | 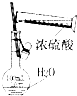 配制100ml 0.1mol•L-1硫酸溶液 | ||
| C. | 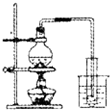 制取少量蒸馏水 | D. | 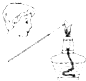 检验钾元素的存在 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 20mL0.3 mol•L-1Na2CO3 | B. | 10mL0.4 mol•L-1Na2CO3 | ||
| C. | 25mL0.4 mol•L-1Na2CO3 | D. | 15mL0.5 mol•L-1Na2CO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | (NH4)2SO4溶于水:(NH4)2SO4═2NH4++SO42- | |
| B. | H3PO4溶于水:H3PO4?3H++PO43- | |
| C. | HF溶于水:HF?H++F- | |
| D. | NaHS溶于水:NaHS═Na++HS- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 负极的反应式为:CH3OH+H2O-6e-═CO2↑+6H+ | |
| B. | 氧气在电极上的反应是O2+4H++4e-═2H2O | |
| C. | 通入甲醇的一极为负极,通入氧气的一极为正极 | |
| D. | 燃料电池的能量转化率能达到100% |
查看答案和解析>>
科目:高中化学 来源:2017届贵州省高三上第四次模拟化学试卷(解析版) 题型:填空题
【化学-选修3:物质结构与性质】
铁、铜及其化合物在日常生产、生活有着广泛的应用。请回答下列问题:
(1)铁在元素周期表中的位置是______________,基态铜原子的核外电子排布式为________________。
(2)配合物Fe(CO)x常温下呈液态,熔点为-20.5℃,沸点为103℃,易溶于非极性溶剂,据此可判断Fe(CO)x晶体属于____________(填晶体类型)。
(3)CO和CO的一种生活中常见等电子体分子,两者相比较沸点较高的为__________(填化学式)。CN-中碳原子杂化轨道类型为_______________,C、N、O三元素的第一电离能最大的为_______________(用元素符号表示)。
(4)铜晶体中铜原子的堆积方式如图1所示。每个铜原子周围距离最近的铜原子数目__________。
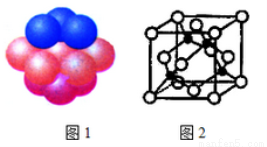
(5)M原子的价电子排布式为3s23p5,铜与M形成化合物的晶胞如图2所示(黑点代表铜原子)。
①该晶体的化学式为_____________。
②已知铜和M的电负性分别为1.9和3.0,则铜与M形成的化合物属于________________(填“离子”、“共价”)化合物。
③已知该晶体的密度为ρg·cm-3,阿伏伽德罗常数为NA,已知该晶体中铜原子和M原子之间的最短距离为体对角线的1/4,则该晶体中铜原子和M原子之间的最短距离为_______________pm(只写计算式)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com