
科学家一直致力于研究常温、常压下“人工固氮”的新方法.曾有报道:在常温、常压、光照条件下,N2在催化剂(掺有少量Fe2O3的TiO2)表面与水发生反应,生成的主要产物为NH3和另一种常见气体.进一步研究NH3生成量与温度的关系(其它条件均相同),部分实验数据见下表:
| T/K | 303 | 313 | 323 |
| 平衡时NH3的生成量/(10﹣6mol) | 4.8 | 5.9 | 6.0 |
回答下列问题:
(1)写出该反应的化学方程式
(2)该反应的焓变△H 0(填“>”、“<”或“=”)
(3)请在答题纸的坐标图中画出上述反应在有催化剂与无催化剂两种情况下反应过程中体系能量变化示意图,并进行必要标注.
(4)与目前广泛使用的工业合成氨方法相比,该方法中固氮反应速率慢.请提出可提高其反应速率且增大NH3生成量的建议: .
(5)已知:
N2(g)+3H2(g)═2NH3(g)△H=﹣92.4kJ/mol
H2(g)+Cl2(g)═2HCl(g)△H=﹣184.6kJ/mol
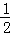 N2(g)+2H2(g)+
N2(g)+2H2(g)+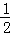 Cl2(g)═NH4Cl(s)△H=﹣313.6kJ/mol
Cl2(g)═NH4Cl(s)△H=﹣313.6kJ/mol
计算NH3(g)+HCl(g)═NH4Cl(s)的反应焓变:△H= .
考点:
反应热和焓变;热化学方程式.
专题:
化学反应中的能量变化.
分析:
(1)根据已知反应物和生成物分析出另一种产物,再利用氧化还原配平法配平;
(2)图表分析温度升高,平衡状态氨气的物质的量增大,说明升温平衡正向进行,正反应为吸热反应;
(3)催化剂是通过降低反应的活化能来加快化学反应速率的;
(4)根据影响化学反应速率的因素和影响平衡的因素来回答;
(5)根据盖斯定律来计算;
解答:
解:(1)已知反应物是N2和H2O生成物有NH3,N2→NH3用氮元素化合价降低,则氧元素化合价一定升高,所以另一种产物为氧气,再根据氧化还原配平法配平方程式为:2N2+6H2O 4NH3+3O2,故答案为:2N2+6H2O
4NH3+3O2,故答案为:2N2+6H2O 4NH3+3O2;
4NH3+3O2;
(2)图表分析温度升高,平衡状态氨气的物质的量增大,说明升温平衡正向进行,正反应为吸热反应,△H>0;
故答案为:>;
(3)催化剂是通过降低反应的活化能来加快化学反应速率的,所以图象为: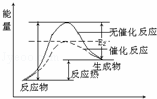 ,故答案为:
,故答案为: ;
;
(4)可提高其反应速率且增大NH3生成量,增大速率,且平衡正移,根据影响化学反应速率的因素和影响平衡的因素可知,升高温度,增大反应物氮气的浓度,能提高其反应速率且平衡正移;
故答案为:升高温度,增大反应物氮气的浓度;
(5)①已知:
N2(g)+3H2(g)═2NH3(g)△H=﹣92.4kJ/mol
H2(g)+Cl2(g)═2HCl(g)△H=﹣184.6kJ/mol
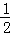 N2(g)+2H2(g)+
N2(g)+2H2(g)+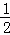 Cl2(g)═NH4Cl(s)△H=﹣313.6kJ/mol;
Cl2(g)═NH4Cl(s)△H=﹣313.6kJ/mol;
把第一个和第二个方程除以2,反写后相加,再与第三个方程相加,则△H=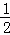 ×92.4kJ/mol+
×92.4kJ/mol+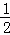 ×184.6kJ/mol+(﹣313.6kJ/mol)=﹣175.1 kJ/mol,
×184.6kJ/mol+(﹣313.6kJ/mol)=﹣175.1 kJ/mol,
故答案为:﹣175.1 kJ/mol;
点评:
本题考查学生化学平衡和化学反应速率的有关知识,以及反应方向的判断,综合性较强,难度中等.


科目:高中化学 来源: 题型:
某同学欲用已知物质的量浓度的盐酸来测定未知物质的量浓度的NaOH溶液时,选择甲基橙作指示剂.请回答下列问题:
(1)用标准的盐酸滴定待测的NaOH溶液时,左手把握酸式滴定管的活塞,右手摇动锥形瓶,眼睛注视 .直到因加入一滴盐酸后,溶液由黄色变为橙色,并 为止.
(2)下列操作中可能使所测NaOH溶液的浓度数值偏低的是 (填字母)
A.酸式滴定管未用标准盐酸润洗就直接注入标准盐酸
B.滴定前盛放NaOH溶液的锥形瓶用蒸馏水洗净后没有干燥
C.酸式滴定管在滴定前有气泡,滴定后气泡消失
D.读取盐酸体积时,开始仰视读数,滴定结束时俯视读数
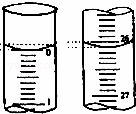
(3)若滴定开始和结束时,酸式滴定管中的液面分别如图所示,则起始读数为 mL,终点读数为 mL;所用盐酸的体 mL.
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组离子,在指定的环境中可能大量共存的是( )
|
| A. | 水电离出来的c(H+)=10﹣13mol/L的溶液:K+、HCO3﹣、Br﹣、Ba2+ |
|
| B. | 滴加石蕊试液显红色的溶液:Fe2+、NH4+、Cl﹣、NO3﹣ |
|
| C. | 与金属铝反应只能放出氢气的溶液:NO3﹣、K+、Cl﹣、Na+、OH﹣ |
|
| D. | c(H+)>c(OH﹣)的溶液中:Na+、K+、SO42﹣、S2﹣ |
查看答案和解析>>
科目:高中化学 来源: 题型:
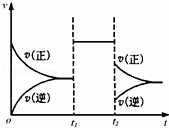
可逆反应aX+2Y(g)⇌2Z(g)在一定条件下达到平衡后,t1和t2时各改变某一种外界条件,化学反应速率(v)﹣时间(t)图象如图.则下列说法正确的是( )
|
| A. | 若X是固体,则t1时一定是增大了容器的压强 |
|
| B. | 若X是气体,则t2时可能是增大了容器的压强 |
|
| C. | 若X是固体,则t1时可能是增大了X的质量 |
|
| D. | t2时不可能是减小容器压强;若采用了降温措施,则该反应的正反应方向△H<0 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列溶液中:①石灰水 ②Na2S溶液 ③KMnO4溶液 ④溴水 ⑤酸化的Ba(NO3)2溶液 ⑥品红溶液,不能区别SO2和CO2气体的是()
A. ②④⑤ B. ①② C. ①②⑤ D. 只有①
查看答案和解析>>
科目:高中化学 来源: 题型:
类推是学习和研究的重要思维方法.下列类推结论正确的是()
化学事实 类推结论
A Al在O2中燃烧生成Al2O3 Fe在O2中燃烧也生成Fe2O3
B pH=3的盐酸稀释1000倍后pH=6 pH=6的盐酸稀释1000倍后pH=9
C 用电解熔融MgCl2的方法冶炼金属镁 用电解熔融NaCl的方法制取金属钠
D 将SO2通入BaCl2溶液中无沉淀生成 将SO2通入Ba(NO3)2溶液中也无沉淀生成
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
A、B、C都是有机化合物,且有如下转化关系:A B
B C,A的相对分子质量比B大2,C的相对分子量比B大16,C能与过量的NaOH反应生成一种常见的气体,以下说法正确的是( )
C,A的相对分子质量比B大2,C的相对分子量比B大16,C能与过量的NaOH反应生成一种常见的气体,以下说法正确的是( )
|
| A. | A是乙炔,B是乙烯 | B. | A是乙烯,B是乙烷 |
|
| C. | A是乙醇,B是乙醛 | D. | A是环己烷,B是苯 |
查看答案和解析>>
科目:高中化学 来源: 题型:
在2 L容器中3种物质间进行反应,X、Y、Z的物质的量随时间的变化曲线如图。反应在t时刻达到平衡,依图所示:
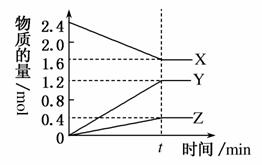
(1)该反应的化学方程式是___________________________。
(2)反应起始至t,Y的平均反应速率是_________________。
(3)X的转化率是_____________________________________。
(4)关于该反应的说法正确的是________。
A.到达t时刻反应已停止
B.在t时刻之前X的消耗速率大于它的生成速率
C.在t时刻正反应速率等于逆反应速率
D.在t时刻达到平衡是因为此时反应物总物质的量与生成物总物质的量相等
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com