
����Ŀ��������Ԫ��A��B��C��D��E��F��ԭ����������������Ԫ��������Ϣ���±���
Ԫ�ر�� | Ԫ��������Ϣ |
A | �����Ӻ������� |
B | ������ۺ�����۵ľ���ֵ֮��Ϊ2 |
C | �������������ڲ��������3�� |
D | 1molD����������ˮ��Ӧ���ڱ�״��������11.2LH2 |
E | ԭ�������������������������� |
F | �����������ӵĵ��Ӳ�ṹ��Arԭ����ͬ |
��1��F�ļ����ӵĽṹʾ��ͼΪ��
��2��E�����ڱ��е�λ��Ϊ��
��3��C��D�����ӵİ뾶��СΪ���������ӷ��ź͡���������=��������ʾ��
��4��Ԫ�طǽ�����ǿ���Ƚ��кܶ��������C��F�ķǽ�����ǿ�����о������в����е���������ţ��� a���Ƚ����ֵ��ʵ���ɫ �� b���Ƚ��⻯����ȶ���
c��������Ԫ�������ڱ��е�λ�� d��������Ԫ�ص�������Ȼ���еĴ���״̬
��5��A��C��D����Ԫ����ɵĻ������к��еĻ�ѧ��Ϊ ��
���𰸡�
��1��![]()
��2���������ڢ�A��
��3��O2����Na+
��4��bc
��5�����ۼ�
���������⣺������Ԫ��A��B��C��D��E��F��ԭ��������������A�������Ӻ������ӣ���AΪHԪ�أ�CԪ��ԭ���������������ڲ��������3��������������������8������2�����Ӳ㣬����������Ϊ6����CΪOԪ�أ�Bԭ��������ۺ�����۵ľ���ֵ֮��Ϊ2������VA�壬ԭ������С��������BΪNԪ�أ�1molD����������ˮ��Ӧ���ڱ�״��������11.2LH2 �� ��������Ϊ0.5mol��D����+1�ۣ�ԭ����������������DΪNa��E��F�����ڵ������ڣ�EԪ��ԭ������������������������������EΪAl��FԪ��ԭ�Ӹ����������ӵĵ��Ӳ�ṹ��Arԭ����ͬ����FΪSԪ�أ���1��F�ļ�����ΪS2�� �� ���ӽṹʾ��ͼΪ ![]() �����Դ��ǣ�
�����Դ��ǣ� ![]() ����2��EΪAlԪ�أ������ڱ��е�λ��Ϊ���������ڢ�A�壬���Դ��ǣ��������ڢ�A�壻��3��C��D�����ӷֱ�ΪO2����Na+ �� ���ߵ��Ӳ�ṹ��ͬ���˵����Խ�����Ӱ뾶ԽС�������Ӱ뾶��O2����Na+ �� ���Դ��ǣ�O2����Na+����4��a�����ʵ���ɫ�����������ʣ����ܱȽϷǽ�����ǿ������a����b���ǽ�����Խǿ���⻯��Խ�ȶ�����b��ȷ��c��ͬ����������ҷǽ����Լ�����ͬ�������϶��·ǽ�������ǿ����c��ȷ�� d����Ԫ�ص�������Ȼ���ж��л���̬������̬�����ܱȽϷǽ�����ǿ������d���� ��ѡ��bc����5��A��C��D����Ԫ����ɵĻ�����Ϊ���ᡢ����淋ȣ�һ�����еĻ�ѧ��Ϊ���ۼ������Դ��ǣ����ۼ���
����2��EΪAlԪ�أ������ڱ��е�λ��Ϊ���������ڢ�A�壬���Դ��ǣ��������ڢ�A�壻��3��C��D�����ӷֱ�ΪO2����Na+ �� ���ߵ��Ӳ�ṹ��ͬ���˵����Խ�����Ӱ뾶ԽС�������Ӱ뾶��O2����Na+ �� ���Դ��ǣ�O2����Na+����4��a�����ʵ���ɫ�����������ʣ����ܱȽϷǽ�����ǿ������a����b���ǽ�����Խǿ���⻯��Խ�ȶ�����b��ȷ��c��ͬ����������ҷǽ����Լ�����ͬ�������϶��·ǽ�������ǿ����c��ȷ�� d����Ԫ�ص�������Ȼ���ж��л���̬������̬�����ܱȽϷǽ�����ǿ������d���� ��ѡ��bc����5��A��C��D����Ԫ����ɵĻ�����Ϊ���ᡢ����淋ȣ�һ�����еĻ�ѧ��Ϊ���ۼ������Դ��ǣ����ۼ���


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������й����ʱ仯��˵������ȷ���ǣ� ��
A. ʯ�͵ķ�����ѻ����ǻ�ѧ�仯 B. ������Ӧ��������Ӧ������ȡ����Ӧ
C. ú��Һ�����������ǻ�ѧ�仯 D. ��ϩ����ˮ��Ӧ�ͱ���H2��Ӧ�����ڼӳɷ�Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������Լ��У������ڼ���ƾ����Ƿ���ˮ �� ��
A. CuSO45H2O B. ��ˮ����ͭ C. ������ D. Ũ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��A��B��C��D��EΪԭ������������������ֶ�����Ԫ�أ����н�����һ�ֽ���Ԫ�أ�A��D������������ͬ��B��C��E�����ڱ������ڣ���C��Eͬ���壮B��C������������֮�͵���D��ԭ�Ӻ����������A��C���γ����ֳ�����Һ̬����� ��ش��������⣺��
��1��B��ԭ�ӽṹʾ��ͼ��
��2��C��D��E����ԭ�Ӷ�Ӧ�����Ӱ뾶�ɴ�С��˳��������������ӣ�����A��B��C����Ԫ�ذ�4��2��3��ɵĻ����������Ļ�ѧ���������� ��
��3����100mL18mol/L��Ũ��A��C��E �������Һ�м��������ͭƬ������ʹ֮��ַ�Ӧ�������������ڱ�״���µ������������������ţ� a��7.32L b��6.72L c��20.16L d��30.24L
��ʹ������Ӧ��ʣ���ͭƬ�����ܽ⣬�������м��������ƣ���Ӧ�����ӷ���ʽΪ�� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��25 ��ʱ����ˮ�м���NaOH��ʹ��Һ��pHΪ11������NaOH�������OH������Ũ����ˮ�����OH������Ũ��֮��Ϊ
A. 1010��1 B. 5��109��1 C. 108��1 D. 1��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����A��B��C��D��E��F��ʾ����10�����ӵ��������ӻ���ӣ�����ش�
��1��A����Ϊ����������Aԭ��������������ԭ�Ӱ뾶���A������
��2��C��������Ԫ����ɵķ��ӣ���ˮ��Һ�ʼ��ԣ������ʽ��
��3��D��������Ԫ����ɵ���ԭ�ӷ��ӣ�����ʽ��
��4����B�м���F�ȳ��ְ�ɫ������������F�����ܽ⣬д���ù��̵����ӷ���ʽ
��5��E+F��C+Dд���÷���ʽ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪�����Ȼ�ѧ����ʽ��
�� 2H2(g)��O2(g)===2H2O(l)��H����570.0 kJ��mol��1
��H2O(g)===H2(g)��![]() O2(g)��H�� +241.8 kJ��mol��1
O2(g)��H�� +241.8 kJ��mol��1
��C(s)��![]() O2(g)===CO(g)��H����110.5 kJ��mol��1
O2(g)===CO(g)��H����110.5 kJ��mol��1
��C(s)��O2(g)===CO2(g) ��H����393.5 kJ��mol��1
�ش����и����⣺
(1)������Ӧ�����ڷ��ȷ�Ӧ����___________________��(����ţ�
(2)H2��ȼ������H��___________________��C��ȼ������H��___________________��
(3)ȼ��10 g H2����Һ̬ˮ���ų�������Ϊ___________________��
(4)�����Ҫ�ͷ�787kJ����������Ҫ��ȫȼ��____________________g��̼��
(5)CO��ȼ������H��____�����Ȼ�ѧ����ʽΪ________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧ�������������������ء�����˵������ȷ����
A. ��ۼӹ���Ӧ���С��Ͻ��̻𡱵�������ͼ��
B. ���ӽ���ǰ�����Ȼ����Һ�������Ӵ�
C. �ô���Ǧ��������ȥ��������ˮ�е�������
D. ��Ӳˮϴ������˷ѷ���Ҳϴ��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��C��D��E��F��X��Y���Ƕ��Ե缫������Դ��ͨ�����ң��е����̪��Һ���� F�������Ժ�ɫ��������˵����ȷ����
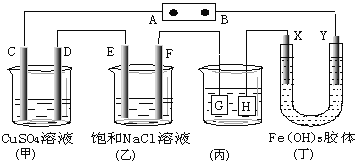
A. �������顢����ȼ�ϵ������Դ�������ΪKOH��Һ����B���ĵ缫��ӦʽΪ��O2��2H2O��4e����4OH��
B. ����(��)װ�ø�ͭ������HӦ����Ag�����Һ��AgNO3��Һ
C. (��)װ����Y���������ɫ���˵���������������������
D. C��D��E��F�缫���е������ɣ������ʵ�����Ϊ1��1��2��2
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com