
已知:NH3·H2O(aq)与H2SO4(aq)反应生成1 mol正盐的ΔH=-24.2 kJ·mol-1;强酸、强碱稀溶液反应的中和热为ΔH=-57.3 kJ·mol-1。则NH3·H2O在水溶液中电离的ΔH等于
A.-69.4 kJ·mol-1 B.-45.2 kJ·mol-1
C.+69.4 kJ·mol-1 D.+45.2 kJ·mol-1
科目:高中化学 来源:2015-2016学年重庆市高一上学期第一次月考化学试卷(解析版) 题型:选择题
设NA为阿伏加德罗常数,下列说法中,正确的是
A.2.4 g金属镁所含电子数目为0.2 NA
B.16 g CH4所含原子数目为NA
C.17 g NH3所含中子数目为10 NA
D.18 g水所含分子数目为NA
查看答案和解析>>
科目:高中化学 来源:2016届重庆市高三上学期10月月考理综化学试卷(解析版) 题型:填空题
(金科选作)(15分)某溶液X中含有H+、Ba2+、Al3+、NH4+、Fe3+、Fe2+、CO32-、SO32-、Cl-、SO42-、NO3-中的几种(除此以外,无其他大量存在的离子),针对该溶液进行实验,内容
如下:
①用洁净的玻璃棒蘸取少量X溶液,点在pH试纸上,试纸呈红色;
②取适量X溶液,加入过量的Ba(NO3)2溶液,得澄清透明的溶液A,并放出一种无色无味的气体B;
③向溶液A中加入过量的NaOH溶液,微热,放出一种刺激性气味的气体C,同时产生红褐色沉淀D,过滤得溶液F;
④向F溶液中通入过量的CO2,有白色沉淀生成。
请回答:
(1) D的化学式为: ;
(2) 检验气体C的方法__________________________________;
(3) 步骤②中反应的离子方程式为: ;
步骤④中反应的离子方程式为: ;
(4) X溶液中一定含有的离子是 ;不能确定是否含有的离子是 ,若要确定该离子(若不至一种,可任选一种)是否存在,最可靠的化学方法是 。
查看答案和解析>>
科目:高中化学 来源:2016届浙江省高三上学期第一次月考化学试卷(解析版) 题型:选择题
下列叙述正确的是
A.阳离子都只有氧化性
B.H2O2既有氧化性,又有还原性,与KMnO4反应时表现H2O2的还原性
C.与强酸、强碱都反应的物质只有两性氧化物或两性氢氧化物
D.分散系中分散质粒子的大小:Fe(OH)3悬浊液<Fe(OH)3胶体<FeCl3溶液
查看答案和解析>>
科目:高中化学 来源:2016届湖南省益阳市高三上学期第三次模拟化学试卷(解析版) 题型:实验题
(12分)锰及化合物在现代工业及有极其重要的用途。
(1)MnO2是一种重要的无机功能材料,蕴藏在海底的丰富的锰结核矿的主要成分是MnO2,工业上从锰结核中制取纯净的MnO2工艺流程如下图所示:
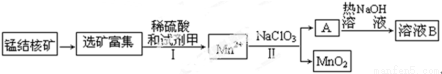
为提高硫酸淋洗效果,需要对富集后的矿石进行处理,处理的内容是_____________,步骤I中,试剂甲必须具有的性质是 。
a.氧化性 b.还原性 c.酸性
(2)步骤Ⅱ中,以NaClO3为氧化剂,当生成0.050 mol MnO2时,消耗0.10 mol·L-1 的NaClO3溶液200 mL ,该反应的离子方程式为__________________________。已知溶液B中的产物之一(Q)可循环用于上述生产,试写出A与NaOH反应的化学方程式_______________________,由于Q可循环利用,有人认为生产中不需要补充物质Q,你是否同意这种看法,理由是_______________。
(3)电解步骤I所得溶液也可得到MnO2,写出生成MnO2的电极反应_______________。
查看答案和解析>>
科目:高中化学 来源:2016届湖南省高三上学期期中测试化学试卷(解析版) 题型:选择题
可能存在的第119号未知元素,有人称为“类钫”,它位于碱金属族,根据周期表结构及元素性质变化趋势,下列关于碱金属某些元素原子的结构和性质的判断,错误的是
①锂与水反应比钠剧烈
②碱金属单质都需要密封保存在煤油中
③锂的氧化物暴露在空气中易吸收二氧化碳
④锂的阳离子的最外层电子数和钠的相同
⑤“类钫”单质是强还原剂
⑥“类钫”在化合物中是+1价
⑦“类钫”单质的密度大于l g·cm-3⑧“类钫”单质有较高的熔点
A.①②④⑧ B.①②③⑦ C.③④⑤⑧ D.①③④⑦
查看答案和解析>>
科目:高中化学 来源:2016届安徽省皖南八校高三上学期第一次联考化学试卷(解析版) 题型:选择题
下列离子方程式中正确的是
A.铜与浓硝酸反应: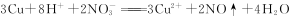
B.向FeBr2溶液中通入足量Cl2: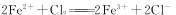
C.AlCl3溶液中加入过量氨水:
D.Ca(HCO3)2溶液中加入少量澄清石灰水: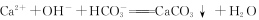
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江苏省高二上期中测试化学试卷(解析版) 题型:选择题
某溶液中存在大量的H+、Clˉ、SO42ˉ,该溶液中还可能大量存在的是
A.OH ˉ B.Ba2+ C.Fe3+ D.CO32ˉ
查看答案和解析>>
科目:高中化学 来源:2015-2016学年安徽省高二上学期第一次月考化学试卷(解析版) 题型:选择题
向足量H2SO4溶液中加入100 mL 0.4 mol·L-1 Ba(OH)2溶液,放出的热量是5.12 kJ。如果向足量Ba(OH)2溶液中加入100 mL 0.4 mol·L-1盐酸时,放出的热量为2.2 kJ。则Na2SO4溶液与BaCl2溶液反应的热化学方程式为
A.Ba2+(aq)+SO42-(aq)=BaSO4(s) ΔH=+73 kJ·mol-1
C.Ba2+(aq)+SO42-(aq)=BaSO4(s) ΔH=-73 kJ·mol-1
B.Ba2+(aq)+SO42-(aq)=BaSO4(s) ΔH=+18 kJ·mol-1
D.Ba2+(aq)+SO42-(aq)=BaSO4(s) ΔH=-18 kJ·mol-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com