
下列叙述中正确的是( )
A.体积相同、浓度均为0.1 mol·L-1的NaOH溶液、氨水,分别稀释m倍、n倍,溶液的pH都变成9,则m<n
B.有甲、乙两氨水溶液,测得甲的pH=a,乙的pH=a+1,则甲乙两溶液c(H+)之比为10:1
C.相同温度下,0.2 mol·L-1乙酸溶液与0.1 mol·L-1乙酸溶液中c(H+)之比为2∶1
D.已知一定温度下,醋酸溶液的物质的量浓度为c,电离度为α,K=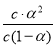 。若加入少量醋酸钠固体,则CH3COOH
。若加入少量醋酸钠固体,则CH3COOH CH3COO-+H+向左移动,α减小,K变小
CH3COO-+H+向左移动,α减小,K变小
科目:高中化学 来源:2016-2017学年山西省高一上10月月考化学试卷(解析版) 题型:选择题
配制一定物质的量浓度的某溶液,下列情况会使配制结果偏低的是
A. 未冷却即转移、定容
B. 未洗烧杯及玻璃棒
C. 定容时俯视刻度线观察液面
D. 容量瓶中原有少量蒸馏水
查看答案和解析>>
科目:高中化学 来源:2016-2017学年黑龙江哈尔滨六中高一上期中化学试卷(解析版) 题型:选择题
已知常温下,在溶液中发生如下反应:
①16H++10Z-+2XO4-=2X2++5Z2+8H2O
②2A2++B2=2A3++2B-
③2B-+Z2=B2+2Z-
由此推断下列说法错误的是( )
A.反应Z2+2A2+=2A3++2Z-可以进行
B.Z元素在反应③中被还原,在反应①中被氧化
C.氧化性由强到弱的顺序是XO4-、Z2、B2、A3+
D.还原性由强到弱的顺序是Z-、B-、A2+、X2+
查看答案和解析>>
科目:高中化学 来源:2016-2017学年黑龙江哈尔滨六中高一上期中化学试卷(解析版) 题型:选择题
为了除去硝酸钾晶体中所含的硫酸钙和硫酸镁,先将它配成溶液,然后先后加入KOH、K2CO3、Ba(NO3)2等试剂,配以过滤、蒸发、结晶等操作,制成纯净的硝酸钾晶体,其加入试剂的顺序正确的是( )
A.K2CO3——Ba(NO3)2——KOH——HNO3
B.Ba(NO3)2——KOH——HNO3——K2CO3
C.KOH——K2CO3——Ba(NO3)2——HNO3
D.Ba(NO3)2——KOH——K2CO3——HN O3
O3
查看答案和解析>>
科目:高中化学 来源:2016-2017学年黑龙江哈尔滨六中高一上期中化学试卷(解析版) 题型:选择题
在蒸馏实验中,下列叙述不正确的是( )
A. 在蒸馏烧瓶中加入约 体积的自来水,并放入几粒碎瓷片
体积的自来水,并放入几粒碎瓷片
B. 蒸馏操作中,烧瓶可直接加热
C. 冷水从冷凝器的下口入,上口出
D. 收集冷凝水时,应弃去开始蒸馏出的部分
查看答案和解析>>
科目:高中化学 来源:2016-2017学年黑龙江哈尔滨六中高二上期中化学试卷(解析版) 题型:选择题
对反应A+3B 2C来说,下列反应速率中最快的是( )
2C来说,下列反应速率中最快的是( )
A.v(A)=0.3 mol/(L·min) B.v(B)=0.6 mol/(L·min)
C.v(C)=0.5 mol/(L·min) D.v(A)=0.01 mol/(L·s)
查看答案和解析>>
科目:高中化学 来源:2016-2017学年黑龙江哈尔滨六中高二上期中化学试卷(解析版) 题型:选择题
若室温时pH=a的氨水与pH=b的盐酸等体积混合,恰好完全反应,则该氨水的电离度可表示为
A.10(a+b-12)% B.10(a+b-14)% C.10(12-a-b)% D.10(14-a-b)%
查看答案和解析>>
科目:高中化学 来源:2016-2017学年黑龙江大庆中学高一上期中化学试卷(解析版) 题型:填空题
(1)现有以下物质:①NaCl固体 ②盐酸 ③Ba(OH)2溶液 ④铜 ⑤二氧化碳气体 ⑥硫酸氢钾固体 ⑦乙醇(C2H5OH) ⑧液态硫酸 ⑨熔融态BaSO4 ⑩液态SO3
请回答下列问题(用序号):
属于电解质的是___________________,属于非电解质的是_______________。
(2)写出下列化学反应的离子方程式
①氢氧化钡溶液和硫酸溶液反应_______________。
②碳酸钙和足量稀盐酸反应_______________。
(3)根据下列离子方程式,各写一个符合条件的化学方程式
HCO3-+H+==CO2↑+H2O_______________。
(4)写出下列物质在水溶液中的电离方程式:
NaHCO3:_______________________________;
查看答案和解析>>
科目:高中化学 来源:2016-2017学年黑龙江大庆中学高二上期中化学试卷(解析版) 题型:选择题
下列热化学方程式能表示可燃物的燃烧热的是( )
A.H2(g)+Cl2(g)=2HCl(g) △H=-184.6kJ/mol
B.CH4(g)+2O2(g )=CO2(g)+2H2O(g) △H=-802.3kJ/mol
)=CO2(g)+2H2O(g) △H=-802.3kJ/mol
C.2C8H18(g)+25O2(g)=16CO2(g)+18H2O(l) △H=-5518kJ/mol
D.CO(g)+1/2O2(g)=CO2(g) △H=-283kJ/mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com