
| A�� | H2SO4��ϡ��$��_{��}^{Cu}$SO2$\stackrel{������ˮ}{��}$NH4HSO3$\stackrel{������ˮ}{��}$��NH4��2SO3 | |
| B�� | NH3$��_{������}^{O_{2}}$NO$\stackrel{O_{2}}{��}$NO2$\stackrel{H_{2}O}{��}$HNO3 | |
| C�� | Fe$��_{��}^{����Cl_{2}}$FeCl2$\stackrel{NaOH��Һ}{��}$Fe��OH��2$\stackrel{�����з���}{��}$Fe��OH��3 | |
| D�� | Al$\stackrel{NaOH��Һ}{��}$NaAlO2$\stackrel{��������}{��}$AlCl3��Һ$\stackrel{��}{��}$��ˮAlCl3 |
���� A��ϡ�����ͭ����Ӧ��
B�������ڴ������¿ɱ���������NO��NO���������ɶ��������������������������
C������������Ӧ�����Ȼ�����
D���Ȼ�����Һ������ˮ����������������
��� �⣺A��ϡ�����ͭ����Ӧ������Ũ�����ڼ�����������ͭ��Ӧ������������������ˮ��Ӧ���ɣ�NH4��2SO3����A����
B�������ڴ������¿ɱ���������NO��NO���������ɶ��������������������������ᣬת����ϵ��ȷ����B��ȷ��
C����������ǿ�����ԣ�����������Ӧ�����Ȼ�������C����
D���Ȼ�����Һ������ˮ����������������������Һ���ܵõ���ˮAlCl3��Ӧ��Ũ���������¼��ȣ���D����
��ѡB��
���� �����ۺϿ���Ԫ�ػ�����֪ʶ��Ϊ��Ƶ���㣬������˫���Ŀ��飬ע��������ʵ������Լ���Ӧ�������ѶȲ���



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����Һ�У�SO2��Cl- K+��HCO3-���Դ������� | |
| B�� | ��FeCl3��Һ��Ӧ�����ӷ���ʽ��S2-+Fe3+�TFe2++S | |
| C�� | ���������ᷴӦ�����ӷ���ʽ��S2-+H+�THS- | |
| D�� | 1L0.1mol•L-1����Һ����������ͭ��Һ��Ӧ����16.0��Cu2S |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A | B | C | D |
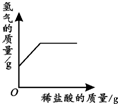
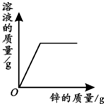
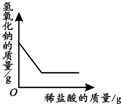
| ��һ���������еμ�ϡ���� | ��һ��������ͭ��Һ�в��ϼ���п�� | ����һ����������ع��� | ��һ������������ ��Һ�еμ�ϡ���� |
 |  |  |  |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ʵ����� | ʵ������ | ʵ����� |
| ��ȡ�����������Թ��У���ˮ�� ֱ����ȫ�ܽ⣮ | �����ݲ��� | ������� |
| ��ȡ�������е���Һ���Թ��У� �μ�CaCl2��Һ�� | ������ɫ���� | ֤����Na2CO3���� |
| �� ȡ�������е���Һ���Թ��У��������CaCl2��Һʹ������ȫ�����ú����ϲ���Һ�еμӷ�̪��Һ�� | ��̪��Һ��� | ֤����NaOH���� |
| �ۺ�����ʵ������˵��������dz����ģ� | ||
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ������Һ������ϴ���۵�ԭ��CO32-+2H2O?H2CO3+2OH- | |
| B�� | ��ǿ����Һ��NaClO��Fe��OH��3��Ӧ�Ʊ�Na2FeO4��3ClO-+2Fe��OH��3+4OH?=2FeO42-+3Cl-+5H2O | |
| C�� | ͭ��Ʒ�����ˮĤ���Խ�ǿʱ�������绯ѧ��ʴ��������ӦΪ2H++2e-=H2�� | |
| D�� | ��AgNO3��Һ�мӹ���NaCl���ټ�Na2S��Һ����ɫ�������ɫ 2Ag++S2-=Ag2S�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 11.2L��a��22.4L | |
| B�� | ��a=16.8L��V��N2O4��=5.6L | |
| C�� | ��a=16.8L��n��NaNO2����n��NaNO3��=4��1 | |
| D�� | �����������NaOH��Һ��Ӧֻ����һ���Σ���n��NO��=0.5mol |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
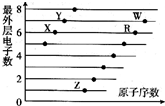
| A�� | ZY��ZW��ˮ��Һ�������� | |
| B�� | ԭ�Ӱ뾶��С��W��R��X�����Ӱ뾶��С��Z+��R2-��W-��Y- | |
| C�� | W���⻯��ˮ��Һ�����Ա�R���⻯��ˮ��Һ������ǿ����֤���ǽ����ԣ�W��R | |
| D�� | Z��X����Ԫ���γɵ�Z2X��Z2X2Ϊ���ӻ����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
 W��X��Y��Z�����ֳ����Ķ�����Ԫ�أ���ԭ�Ӱ뾶��ԭ�������仯��ͼ��ʾ����֪W��һ�ֺ��ص�������Ϊ18��������Ϊ10��X��Neԭ�ӵĺ�����������l��Y�ĵ�����һ�ֳ����İ뵼����ϣ�Z�ķǽ�������ͬ����Ԫ������ǿ������˵������ȷ���ǣ�������
W��X��Y��Z�����ֳ����Ķ�����Ԫ�أ���ԭ�Ӱ뾶��ԭ�������仯��ͼ��ʾ����֪W��һ�ֺ��ص�������Ϊ18��������Ϊ10��X��Neԭ�ӵĺ�����������l��Y�ĵ�����һ�ֳ����İ뵼����ϣ�Z�ķǽ�������ͬ����Ԫ������ǿ������˵������ȷ���ǣ�������| A�� | ��Ӧ�����Ӱ뾶��W��X | |
| B�� | ��Ӧ��̬�⻯����ȶ��ԣ�Y��Z | |
| C�� | ������XZW�Ⱥ����Ӽ����ֺ����ۼ� | |
| D�� | Z���⻯���X������������Ӧˮ�������Һ������Y�������ﷴӦ |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com