
| A. | 中子数为78 | B. | 质子数为53 | C. | 质量数为131 | D. | 核外电子数是78 |
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:填空题
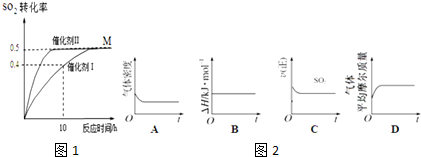
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用酸性高锰酸钾溶液鉴别苯、甲苯和环己烯 | |
| B. | 用燃烧法鉴别乙醇、苯和四氯化碳 | |
| C. | 用水鉴别乙醇、甲苯和溴苯 | |
| D. | 用碳酸钠溶液鉴别乙醇、乙酸和乙酸乙酯 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
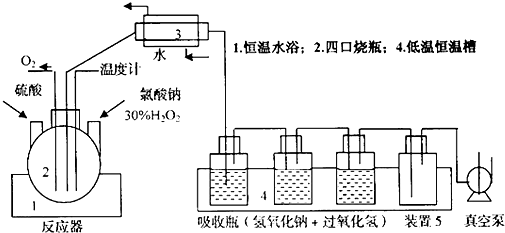
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子半径X>Y>Z | B. | 非金属性X>Y>Z | ||
| C. | 气态氢化物的稳定性HX<H2Y<H3Z | D. | 原子序数 X<Y<Z |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | IBr的电子式为  | |
| B. | HClO的结构式为H-O-Cl | |
| C. | HIO各原子都满足8电子结构 | |
| D. | 共价化合物内部可能有极性键和非极性键 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 中和滴定实验中,如用于装标准液的滴定管洗净、干燥后,未经润洗,测定结果偏高 | |
| B. | 实验室从海带提取单质碘的方法是:取样→灼烧→溶解→过滤→萃取 | |
| C. | 纸层析实验中若选择水做固定相,有机溶剂做流动相,则亲水性强的成分在流动相中分配的少一些,在毛细现象作用下,随流动相移动的速度快一些 | |
| D. | 检验新鲜鸡血中的铁元素时,可在鸡血中加入稀硝酸并加热搅拌蒸干得到固体粉末,取少许粉末加入亚铁氰化钾稀溶液,可得蓝色溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com