
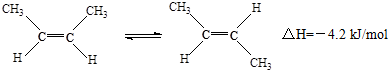
| A. | 顺-2-丁烯比反-2-丁烯稳定 | |
| B. | 顺-2-丁烯的燃烧热比反-2-丁烯大 | |
| C. | 加压和降温有利于平衡向生成顺-2-丁烯反应方向移动 | |
| D. | 它们与氢气加成反应后的产物具有不同的沸点 |
分析 A.物质具有的能量越低越稳定;
B.若生成物相同,反应物的能量高,则放出的热量多;
C.加压平衡箱物质的量减小的方向移动;
D.反-2-丁烯和顺-2-丁烯与氢气加成生成同一种物质.
解答 解:A.顺-2-丁烯转化为反-2-丁烯放热,说明反-2-丁烯能量低,更稳定,故A错误;
B.等量的顺-2-丁烯具有更高的能量.所以顺-2-丁烯燃烧热更大,故B正确;
C.该反应反应前后物质的量相等,加压对顺、反2-丁烯的转化无影响,降温则是有利反-2-丁烯的生成,故C错误;
D.反-2-丁烯和顺-2-丁烯与氢气加成都生成丁烷,所以二者与氢气加成反应后的产物具有相同的沸点,故D错误;
故选B.
点评 本题考查了化学平衡及其影响、反应热与焓变的应用,题目难度不大,明确反应热与焓变的关系为解答关键,注意掌握化学平衡及其影响因素,试题培养了学生的灵活应用能力.


 名校练考卷期末冲刺卷系列答案
名校练考卷期末冲刺卷系列答案科目:高中化学 来源: 题型:解答题
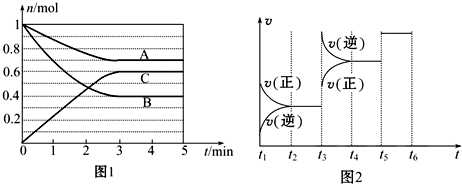
| t2~t3 | t4~t5 | t5~t6 |
| K1 | K2 | K3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
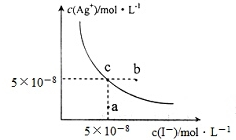
| A. | 在t℃时,Agl的Ksp=2.5×10-15 | |
| B. | 图中b点有碘化银晶体析出 | |
| C. | 向c点溶液中加入适量蒸馏水,可使溶液由c点到a点 | |
| D. | 在t℃时,反应AgBr(s)+I-(aq)?Agl(s)+Br-(aq)的平衡常数K=200 |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
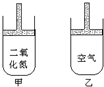 常温常压下在可移动活塞的甲、乙容器(如图)里分别充有等体积的二氧化氮(已建立了平衡:2NO2?N2O4;△H<0.)和空气,现分别进行下列两个实验:
常温常压下在可移动活塞的甲、乙容器(如图)里分别充有等体积的二氧化氮(已建立了平衡:2NO2?N2O4;△H<0.)和空气,现分别进行下列两个实验:| A. | ①甲>乙②甲>乙 | B. | ①甲>乙②甲<乙 | C. | ①甲<乙②甲>乙 | D. | ①甲>乙②甲=乙 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
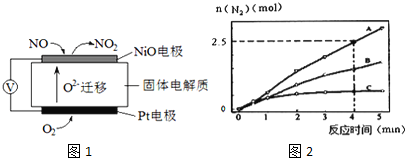
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 溶液 | B. | 悬浊液 | C. | 乳浊液 | D. | 胶体 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com