
| A�� | ��1����2����С��c1��c2������ | B�� | ��1����2������c1��c2����С | ||
| C�� | ��1��С����2����c1��c2������ | D�� | ��1��С����2����c1����c2��С |
���� ���¶Ȳ��������£������ӷ�Ӧ������ʵ�������������������£��൱������ѹǿ���ɴ˷������
��� �⣺���¶Ȳ��������£������ӷ�Ӧ������ʵ�������������������£��൱������ѹǿ���Է�ӦN2O4��g��?2NO2��g��������ѹǿƽ�������ƶ������Ԧ�1��С������Ӧ3O2��g��?2O3��g������ѹǿ��ƽ�������ƶ������Ԧ�2����ƽ��ʱ��Ӧ����������Ũ�ȶ�ԭƽ���Ũ�ȴ���c1��c2������ѡC��
���� ���⿼���˻�ѧƽ��Ӱ�����ط����жϣ���ѧƽ���ƶ�ԭ���ͷ��������ǽ���ؼ�����Ŀ�Ѷ��еȣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��һС����ֽ���ڱ������ϣ��ò�����պȡ��������Һ������ֽ�ϣ��������ɫ������ | |
| B�� | ��ɫ��Һ�м�Ba��NO3��2��Һ���ټ�ϡ���ᣬ�������ܽ⣬����˵��ԭ��Һ��һ����SO42- | |
| C�� | ����ʱ������ƿ��Һ���������ܳ����ݻ���$\frac{2}{3}$��Һ��Ҳ�������� | |
| D�� | �������������ƿ���ܽⲢϡ�����̶ȣ����Ƴ�һ�����ʵ���Ũ�ȵ���Һ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
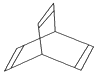 ��һ���л���X�ļ���ʽ��ͼ��ʾ��
��һ���л���X�ļ���ʽ��ͼ��ʾ��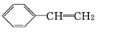 ��
�� ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 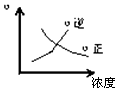 | B�� | 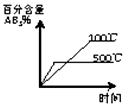 | C�� | 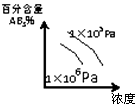 | D�� |  |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ������������������֮��Ϊ136 | |
| B�� | �Ԫ��λ��Ԫ�����ڱ��е������ڢ��� | |
| C�� | ����ķ���ʽΪRn2 | |
| D�� | �Ԫ�������ȶ�������������Ԫ�ػ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �����£�1L 0.1mol/L HCl��Һ�к���ԭ������0.1NA | |
| B�� | ��״���£�2.24L��CO2��O2��ɵĻ�������к�����������0.1NA | |
| C�� | 10g̼�����������ϡ�����ַ�Ӧ���ĵ���������Ϊ0.1NA | |
| D�� | ��״���£�11.2L CO�� NO�����������11.2LN2�з�������Ϊ0.5NA |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com