
| A. | NaHCO3可用于中和胃酸过多 | |
| B. | 硅用于制造光导纤维 | |
| C. | 氯气与澄清石灰水反应制漂白粉 | |
| D. | 医疗上通常直接用无水乙醇进行消毒 |
 巧学巧练系列答案
巧学巧练系列答案 课课练江苏系列答案
课课练江苏系列答案科目:高中化学 来源: 题型:选择题
| A. | CaCl2 | B. | Ba(OH)2 | C. | H2SO4 | D. | HCl |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
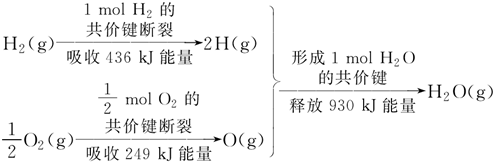
| A. | 1 mol H2的共价键形成放出436 kJ能量 | |
| B. | 氢气跟氧气反应生成水的同时吸收能量 | |
| C. | 1 mol H2(g)跟$\frac{1}{2}$ mol O2(g)反应生成1 mol H2O(g)释放能量245 kJ | |
| D. | 1 mol H2(g)与$\frac{1}{2}$ mol O2(g)的总能量大于1 mol H2O(g)的能量 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 过滤时,漏斗下端紧贴烧杯内壁 | |
| B. | 向试管中滴加液体时,胶头滴管紧贴试管内壁 | |
| C. | 不慎将油汤洒在衣服上可用酒精、汽油等除去,它们能将油污从汤液中萃取出来而除去 | |
| D. | 玻璃是用石灰石,纯碱和二氧化硅等原料熔炼而成,在熔炼过程中发生了化学变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
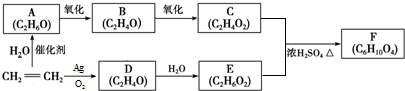
 .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:填空题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
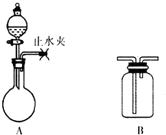 化学是一门以实验为基础的学科.
化学是一门以实验为基础的学科.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com