
| A. | ②④⑤⑧⑨ | B. | ①③⑥⑦⑨ | C. | ①③⑤⑥⑦ | D. | ①②③⑤⑥⑦ |
分析 电子跃迁本质上是组成物质的粒子(原子、离子或分子)中电子的一种能量变化.激光、霓虹灯广告、燃烧、节日里燃放的焰火都与电子发生跃迁释放能量有关.
解答 解:①霓虹灯发出有色光,因为灯泡中的稀有气体原子吸收能量,电子发生跃迁,发射出不同的光,故正确;
②棱镜分光是由于不同色彩的光在玻璃中的折射率不同引起的,与电子跃迁无关,故错误;
③激光的产生就是在外部刺激的情况下,很多高能的电子同时释放相位和能级相同能量,这些能量成为颜色一样的光子,有的在激光器内反射,继续与电子碰撞,释放更多的与它相同的光子,有的离开激光器,形成激光,与电子跃迁有关,故正确;
④石油蒸馏是利用石油中各成分的沸点不同加以分离,与电子跃迁无关,故错误;
⑤凸透镜聚光是由光的折射形成的,与电子跃迁无关,故错误;
⑥燃放的焰火,是因为不同金属离子吸收能量,电子发生跃迁,形成不同的颜色的光,故正确;
⑦日光灯通电发光,是因为电子受到激发的时候原子就会释放出可见光子形成的,与电子跃迁有关,故正确;
⑧冷却结晶,是由于温度降低,溶液的溶解度减小,析出溶质,与电子跃迁无关,故错误;
⑨焰色反应,是因为金属离子吸收能量,电子发生跃迁,形成不同的颜色的光,与电子跃迁有关,故正确.
故选B.
点评 本题考查电子的跃迁,题目难度不大,注意光的形成与电子的跃迁的关系,学习中注意相关知识的积累.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
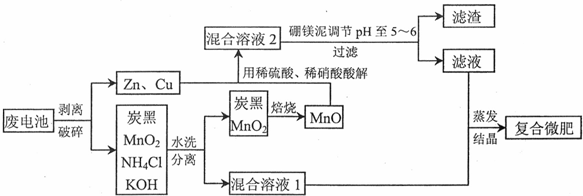
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 2NaOH+H2SO4=NaSO4+2H2O | B. | Ba(OH)2+2 HCl=BaCl2+2H2O | ||
| C. | Ba(OH)2+H2SO4=BaSO4↓+2H2O | D. | Na2CO3+H2SO4=Na2SO4+2H2O+CO2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 10℃20 mL 3mol/L的X溶液 | B. | 20℃30 mL 2molL的X溶液 | ||
| C. | 20℃10 mL 4mol/L的X溶液 | D. | 10℃10 mL 2mol/L的X溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 +CH3CH2OH$?_{△}^{浓硫酸}$
+CH3CH2OH$?_{△}^{浓硫酸}$ +H2O.
+H2O. +2Na2CO3→
+2Na2CO3→ +2NaHCO3.
+2NaHCO3. .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com