
 (4)2CO2 + 2 H2O + SiO32—=2 HCO3—+ H2SiO3↓
(4)2CO2 + 2 H2O + SiO32—=2 HCO3—+ H2SiO3↓ 。
。

科目:高中化学 来源:不详 题型:推断题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.制半导体的材料 | B.耐高温、耐腐蚀的合金材料 |
| C.制农药的材料 | D.制催化剂的材料 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.热稳定性:CH4> SiH4 >HF | B.原子半径:Na>Mg>O |
| C.酸性:HClO4>H2SO4>H3PO4 | D.非金属性:F>Cl>Br |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
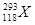 的发现是世界重大科技成果之一,它有力地支持了“稳定岛”(具有“魔数”数目的质子和中子的原子核的化学元素特别稳定)的假说,原子
的发现是世界重大科技成果之一,它有力地支持了“稳定岛”(具有“魔数”数目的质子和中子的原子核的化学元素特别稳定)的假说,原子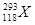 的中子数与核外电子数之差为
的中子数与核外电子数之差为| A.0 | B.118 |
| C.57 | D.175 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.HF、HCl、HBr、HI的热稳定性依次减弱 |
| B.熔点:Li> Na> K> Rb |
| C.NaF、NaCl、NaBr、NaI的熔点依次降低 |
| D.H2S的熔沸点小于H2O的熔沸点 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com