
����Ŀ���������̼�Ȼ�ԭұ��þ�������̵ĵ��ʻ�Ͻ����ν�ҵ���ȵ�֮һ���ش��������⣺
(1)��֪��ϵ�����ܱ仯![]() ʱ��Ӧ���Է����С�
ʱ��Ӧ���Է����С�![]() ���̼�Ȼ�ԭұ��þ����Ҫ��ӦΪ
���̼�Ȼ�ԭұ��þ����Ҫ��ӦΪ![]() ���������ܱ仯���¶ȡ�ѹǿ�Ĺ�ϵ��ͼ��ʾ��
���������ܱ仯���¶ȡ�ѹǿ�Ĺ�ϵ��ͼ��ʾ��

�¶��ɵ͵��ߵ�˳����_______________��![]() ʱ�÷�Ӧ�����Է����е��¶���_________(����
ʱ�÷�Ӧ�����Է����е��¶���_________(����![]() ����
����![]() ������
������![]() ��)��
��)��
(2)![]() �����̼�Ȼ�ԭ
�����̼�Ȼ�ԭ![]() ұ��
ұ��![]() �Ļ������£�
�Ļ������£�
(��)![]()
(��)![]()
(��)![]()
��Ӧ![]() ��
��![]() ______________
______________![]() (�ú�a��b��c�Ĵ���ʽ��ʾ)���м���֮һ
(�ú�a��b��c�Ĵ���ʽ��ʾ)���м���֮һ![]() ��
��![]() ��Ӧ������ʵ�����Ʊ����飬д��
��Ӧ������ʵ�����Ʊ����飬д��![]() ��
��![]() ��Ӧ�Ļ�ѧ����ʽ��_________________________________________________________��
��Ӧ�Ļ�ѧ����ʽ��_________________________________________________________��
(3)�Ʊ��̺Ͻ����ط�Ӧ��ƽ��ʱ![]() ���¶ȵĹ�ϵ��ͼ��ʾ(
���¶ȵĹ�ϵ��ͼ��ʾ(![]() Ϊ�÷�ѹ��ʾ��ƽ�ⳣ������ѹ=��ѹ���������)��
Ϊ�÷�ѹ��ʾ��ƽ�ⳣ������ѹ=��ѹ���������)��
(��)![]()
(��)![]()
(��)![]()
��![]() �ķ�Ӧ��___________(����)��
�ķ�Ӧ��___________(����)��
��![]() ____________[��
____________[��![]() ��
��![]() ��ʾ]��A��
��ʾ]��A��![]() ___________��[
___________��[![]() ��ʾ]��
��ʾ]��
����ij�����ܱ������г���![]() ����������
����������![]() ����ֻ������Ӧ��
����ֻ������Ӧ��![]() ���ﵽB���ƽ��״̬���ﵽƽ��ǰ��v(��)__________v(��)(������������С��������������)���ﵽƽ��ʱ��
���ﵽB���ƽ��״̬���ﵽƽ��ǰ��v(��)__________v(��)(������������С��������������)���ﵽƽ��ʱ��![]() _______________(����С�������λ)��
_______________(����С�������λ)��

���𰸡�![]()
![]()
![]()
![]() ��
�� ![]()
![]() �� 0.13mol
�� 0.13mol
��������
(1).Ҫʹ��Ӧ���Է����У���![]() �����ڷ�Ӧ
�����ڷ�Ӧ![]() ��˵����ӦΪ���ȷ�Ӧ�������ķ�Ӧ����Ӧ�ڽϸ��¶Ȳ����Է����У�
��˵����ӦΪ���ȷ�Ӧ�������ķ�Ӧ����Ӧ�ڽϸ��¶Ȳ����Է����У�
(2).���ø�˹���ɽ��
(3).��ͼ��֪�������¶Ȣ��![]() ��С��˵�������¶�ƽ�������ƶ�������ӦΪ���ȷ�Ӧ���ɸ�˹���ɿ�֪��Ӧ�����ɷ�Ӧ���3����õ���B��ʱ
��С��˵�������¶�ƽ�������ƶ�������ӦΪ���ȷ�Ӧ���ɸ�˹���ɿ�֪��Ӧ�����ɷ�Ӧ���3����õ���B��ʱ![]() =0��˵��p(CO)=p(CO2)���ݴ˽��
=0��˵��p(CO)=p(CO2)���ݴ˽��
(1).�ɷ�����֪����Ӧ�ڽϸ��¶Ȳ����Է����У�GԽС���Է��̶�Խ�ߣ�����![]() ����
����![]() ֻ��T1�¶��µ�G����0���ʴ�Ϊ��
ֻ��T1�¶��µ�G����0���ʴ�Ϊ��![]() ��T1��
��T1��
(2).�ɸ�˹���ɿɵã���Ӧ![]() =
=![]() ����H=
����H=![]() =
=![]()
![]() ��
��![]() ��
��![]() ��Ӧ������ʵ�����Ʊ����飬��ӦΪ��
��Ӧ������ʵ�����Ʊ����飬��ӦΪ��![]() ���ʴ�Ϊ��
���ʴ�Ϊ��![]() ��
��![]() ��
��
(3)���ɷ�����֪:�����¶Ȣ��![]() ��С��˵�������¶�ƽ�������ƶ�������ӦΪ���ȷ�Ӧ��
��С��˵�������¶�ƽ�������ƶ�������ӦΪ���ȷ�Ӧ��
��.�ɸ�˹���ɿ�֪��Ӧ�����ɷ�Ӧ���span>3����õ�����![]() =
=![]() ���ɷ���ʽ��֪��
���ɷ���ʽ��֪��![]() =
=![]() ��
��![]() =
=![]() =
=![]() ��p(CO)�� ��p(CO)=
��p(CO)�� ��p(CO)= ![]() ���ʴ�Ϊ��
���ʴ�Ϊ��![]() ��
��![]() ��
��
��. p(CO)= 2p(CO2)����B��ʱ![]() =0����p(CO)= p(CO2)����ʼʱ��Ҫʹp(CO)= p(CO2)��ƽ�������ƶ�����v(��)�� v(��)����CO2ת��x����Ϊ��Ӧ������У���������ʽ�У�
=0����p(CO)= p(CO2)����ʼʱ��Ҫʹp(CO)= p(CO2)��ƽ�������ƶ�����v(��)�� v(��)����CO2ת��x����Ϊ��Ӧ������У���������ʽ�У�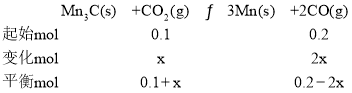 ����ΪB��ʱp(CO)= p(CO2)���а���٤����������ѹǿ֮�ȵ������ʵ���֮�ȣ���0.1+x=0.2-2x��x=
����ΪB��ʱp(CO)= p(CO2)���а���٤����������ѹǿ֮�ȵ������ʵ���֮�ȣ���0.1+x=0.2-2x��x=![]() ������ƽ��ʱ��һ����̼�ĵ�ʣ����Ϊ0.13mol���ʴ�Ϊ������0.13mol��
������ƽ��ʱ��һ����̼�ĵ�ʣ����Ϊ0.13mol���ʴ�Ϊ������0.13mol��


 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������(��H3R��ʾ)��һ�ָ�Ч������������ʱ����һ��Ũ�ȵ���������Һȥ��ˮ������Һ��H3R��H2R-��HR2-��R3-�����ʵ����ٷ�����pH�ı仯��ͼ��ʾ������˵����ȷ����
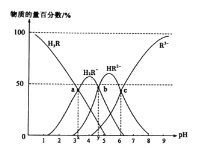
A.��a���ж�H3R�ĵ�һ�����볣��Ka1(H3R)��������Ϊ10-3
B.��b����Һ�н���������ֻ��Na+������c(Na+)=c(R3-)+c(HR2-)+c(H2R-)+c(H3R)
C.pH=6ʱ��c(R3-)=c(HR2-)>c(H+)>c(OH-)
D.��Ӧ2H2R-![]() H3R+HR2-�ڸ��¶��µ�ƽ�ⳣ��K=10x-y
H3R+HR2-�ڸ��¶��µ�ƽ�ⳣ��K=10x-y
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й����л����˵����ȷ����
A.�Ҵ��ͱ�������Ϊͬϵ��
B.����ϩ��![]() �������е�����̼ԭ�ӹ���
�������е�����̼ԭ�ӹ���
C.����ʽΪC5H10O2,����������ͬ���칹�干��9�֣������������칹��
D.�Ż�������[2,2,0]��![]() ���Ķ��ȴ�����6�ֽṹ�������������칹��
���Ķ��ȴ�����6�ֽṹ�������������칹��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���Ȼ���������![]() �������õ������������Ư�����á�ʪ������������ֽ���ʯ�õ������к�Fe3+��Al3+�����ʡ���ʪ������Ϊԭ����ȡ�Ȼ��������ƵĹ����������£�
�������õ������������Ư�����á�ʪ������������ֽ���ʯ�õ������к�Fe3+��Al3+�����ʡ���ʪ������Ϊԭ����ȡ�Ȼ��������ƵĹ����������£�
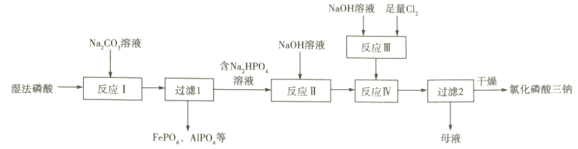
��֪��a���¶ȸ�ʱ��NaClO�ֽ⡣
b�������£���������ֲַ�������pH�Ĺ�ϵ����ͼ��ʾ��
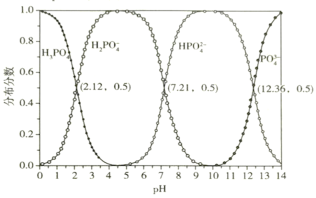
�ش��������⣺
(1)����ֽ�Ca5(PO4)3Fʱ�������ж�������Ҫ��________________(�ѧʽ)��
(2)��Ӧ��������ת��Ϊ���Σ�����������Fe3+��Al3+�����γɳ�����
�ٷ�Ӧ���з��������Ӧ����������ת��ΪNa2HPO4����Ҫ���ӷ���ʽΪ___________��������Ӧ����pHԼΪ_____________________________��
�ڳ����£�HPO![]() +Fe3+
+Fe3+![]() FePO4+H+��lgKΪ_________
FePO4+H+��lgKΪ_________![]() ��
��
(3)��Ӧ���в���Na2CO3��Һ��ԭ����____________________________________________��
(4)��Ӧ���Ļ�ѧ����ʽΪ____________________________________________��
��Ӧ����������Һ��Ϻ��������ȴ����Ŀ����____________________________��
��ĸҺ���е�������NaClO��_____________________(��2��)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijѧϰС�����÷�Ӧ ��ȡ
��ȡ![]() ��Һ��ʵ��װ����ͼ��ʾ(��֪��
��Һ��ʵ��װ����ͼ��ʾ(��֪�� )����˵����ȷ����( )
)����˵����ȷ����( )

A.װ��b�п�ʢ��������Ũ![]() ��Һ
��Һ
B.װ��c���ʵļ��ȷ�ʽ����ˮԡ
C.��Ӧ��ȡ����װ��c����Һ���μ�![]() ��Һ���л�ɫ�������ɣ�˵��
��Һ���л�ɫ�������ɣ�˵��![]() ����ԭ
����ԭ
D.��װ��e����Һδ�����ǣ�˵����ʵ��������һ��û��![]() ����
����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����н�����ʵ�ķ���ʽ����ȷ����
A. ��Na2S������Hg2+��ˮ��Hg2+ + S2 = HgS��
B. ȼú��������ʯ�Ҽ���SO2���ŷţ�2CaO + O2 + 2SO2 ![]() 2CaSO4
2CaSO4
C. ��ҵ�Ͻ�Cl2 ͨ��ʯ��������Ư�ۣ�Cl2 + OH�� = Cl��+ ClO�� + H2O
D. ��Ư��Һ�м�����������飨�����ᣩ������������ClO��+ Cl��+2H�� = Cl2��+ H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪�Ȼ�ѧ����ʽ��H2O(g)=H2(g)+![]() O2(g) ��H= +241.8kJ/mol��H2(g)+
O2(g) ��H= +241.8kJ/mol��H2(g)+![]() O2(g)=H2O(1) ��H= -285.8kJ/mol
O2(g)=H2O(1) ��H= -285.8kJ/mol
��1gˮ������ΪҺ̬ˮʱ�����ʱ�Ϊ
A.��H= +4.4kJ/molB.��H= -4.4kJ/mol
C.��H= -2.44kJ/molD.��H= +2.44kJ/mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й����Ȼ�ѧ��Ӧ����������ȷ����
A. HCl��NaOH��Ӧ���к�����H����57.3kJ/mol����H2SO4��Ca(OH)2��Ӧ���к�����H��2��(��57.3)kJ/mol
B. CO(g)��ȼ������283.0kJ/mol����2CO2(g) ��2CO(g)��O2(g)��Ӧ����H��+2��283.0kJ/mol
C. ��Ҫ���Ȳ��ܷ����ķ�Ӧһ�������ȷ�Ӧ
D. 1mol����ȼ��������̬ˮ�Ͷ�����̼���ų��������Ǽ����ȼ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ͨ���Ȼ�ѧѭ���ڽϵ��¶�����ˮ������ֽ��Ʊ������ķ�Ӧϵͳԭ����

��1��ͨ�����㣬��֪ϵͳ��I����ϵͳ��II��������Ȼ�ѧ����ʽ�ֱ�Ϊ__________________ ��______________________���Ƶõ���H2�����������ٵ���___________��
��2��H2S��CO2�ڸ����·�����Ӧ��H2S(g)+CO2(g)![]() COS(g)+H2O(g)����610Kʱ����0.10 mol CO2��0.40 mol H2S����2.5 L�Ŀո�ƿ�У���Ӧƽ���ˮ�����ʵ�������Ϊ0.02��
COS(g)+H2O(g)����610Kʱ����0.10 mol CO2��0.40 mol H2S����2.5 L�Ŀո�ƿ�У���Ӧƽ���ˮ�����ʵ�������Ϊ0.02��
��H2S��ƽ��ת����a1=_____ %����Ӧƽ�ⳣ��K =___________��
����620K�ظ�ʵ�飬ƽ���ˮ�����ʵ�������Ϊ0.03��H2S��ת����a2 _____________a1���÷�Ӧ��H __________0�����>�� ��<�� ��=����
����Ӧ�����ٷֱ�����������壬��ʹH2Sת����������� _____ �����ţ���
A.H2S B.CO2 C.COS D.N2
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com