

分析 探究SO2气体还原Fe3+、I2,由实验装置可知,A中发生SO2+2Fe3++2H2O═2Fe2++SO42-+4H+,B中发生I2+SO2+2H2O=2I-+SO42-+4H+,C中NaOH溶液可吸收过量的二氧化硫,A中SO2、Fe2+均能与高锰酸钾发生氧化还原反应,而Fe3+与KSCN溶液反应溶液为血红色,以此来解答.
解答 解:(1)装置A中SO2做还原剂,被氧化为硫酸根离子,Fe3+作氧化剂,被还原为Fe2+,反应离子方程式为SO2+2Fe3++2H2O═2Fe2++SO42-+4H+,则A中反应的现象为溶液颜色由黄色逐渐变为浅绿色,由反应可知SO2和Fe3+的物质的量之比是1:2,
故答案为:溶液颜色由黄色逐渐变为浅绿色;1:2;
(2)B中二氧化硫被碘单质氧化生成硫酸和碘化氢,离子方程式为I2+SO2+2H2O=2I-+SO42-+4H+,
故答案为:I2+SO2+2H2O=2I-+SO42-+4H+;
(3)二氧化硫有还原性,高锰酸钾有强氧化性,二氧化硫能与高锰酸钾发生氧化还原反应使高锰酸钾溶液褪色,Fe2+也使高锰酸钾溶液褪色,则方案①不合理,但②中Fe3+与KSCN溶液反应溶液为血红色,亚铁离子与氯水反应生成铁离子,溶液变红,可验证A中SO2与Fe3+发生了氧化还原反应,
故答案为:方案①;SO2、Fe2+均能与高锰酸钾发生氧化还原反应.
点评 本题考查性质实验方案的设计,为高频考点,把握图中实验装置的作用、物质的性质及发生的反应为解答的关键,侧重分析与实验能力的考查,注意元素化合物知识与实验的结合,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 加热能杀死流感病毒是因为蛋白质受热变性 | |
| B. | 海轮船体镶嵌锌块是牺牲阳极的阴极保护法,防止船体被腐蚀 | |
| C. | 氢氧化铝和碳酸钠均可用于治疗胃酸过多 | |
| D. | 食用油反复加热会产生稠环芳烃等有害物质 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 分子中有1个手性碳原子 | B. | 遇FeCl3溶液显紫色 | ||
| C. | 1mol杀鼠灵最多能与9molH2反应 | D. | 能萃取碘水中的碘单质 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题


查看答案和解析>>
科目:高中化学 来源: 题型:解答题
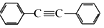 以互为同系物的单取代芳烃A、G为原料合成M的一种路线(部分反应条件略去)如图:
以互为同系物的单取代芳烃A、G为原料合成M的一种路线(部分反应条件略去)如图:
 ,B的官能团名称为羰基.
,B的官能团名称为羰基. .
. .
. 或
或 .
. 的合成路线:
的合成路线: .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
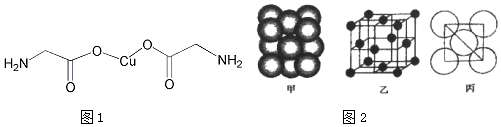
 世界上最早现并使用锌的是中国,明朝末年《天工开物》一书中有世界上最早的关于炼锌技术的记载.回答下列问題:
世界上最早现并使用锌的是中国,明朝末年《天工开物》一书中有世界上最早的关于炼锌技术的记载.回答下列问題:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | pH=4的氯化铵溶液中:c(H+)=c(NH3•H2O )=1×10-4mol•L-1 | |
| B. | pH相同的①NaOH、②NaClO两种溶液中水的电离程度:①<② | |
| C. | pH=2的HF溶液与pH=12的NaOH溶液以体积比1:1混合:c(Na+)=c(F-)>c(H+)=c(OH-) | |
| D. | pH=a的HCl溶液,稀释10倍后,其pH=b,则a=b-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲烷分子中的4个C-H键完全相等 | B. | CH3Cl 只有1种 | ||
| C. | CH2Cl2不存在同分异构体 | D. | CHCl3不存在同分异构体 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com