
| A£® | ¾§ĢåŌŚŹÜČČČŪ»Æ¹ż³ĢÖŠŅ»¶Ø“ęŌŚ»Æѧ¼üµÄ¶ĻĮŃ | |
| B£® | ¾§ĢåµÄ×Ō·¶ŠŌŹĒÖøŌŚŹŹŅĖĢõ¼žĻĀ¾§ĢåÄܹ»×Ō·¢µŲ³ŹĻÖ¹ęŌņµÄ¶ąĆęĢåĶāŠĪ | |
| C£® | Ēų·Ö¾§ĢåŗĶ·Ē¾§Ģå×īæĘѧµÄ·½·ØŹĒ¶Ō¹ĢĢå½ųŠŠX-ÉäĻßŃÜÉ䏵Ńé | |
| D£® | ¾§ĢåµÄø÷ĻņŅģŠŌČ”¾öÓŚĪ¢¹ŪĮ£×ÓµÄÅÅĮŠ¾ßÓŠĢŲ¶ØµÄ·½ĻņŠŌ |
·ÖĪö A”¢·Ö×Ó¾§ĢåČŪ»ÆŹ±Ņ»°ćĘĘ»µ·Ö×Ó¼ä×÷ÓĆĮ¦£¬¶ų²»Ó°Ļģ»Æѧ¼ü£»
B”¢¾§ĢåŌŚ¹ĢĢ¬Ź±²»¾ßÓŠ×Ō·¢ŠŌ£¬²»ÄÜŠĪ³ÉŠĀµÄ¾§Ģ壻
C”¢¹¹³É¾§ĢåµÄĮ£×ÓŌŚĪ¢¹ŪæÕ¼äĄļ³ŹĻÖÖÜĘŚŠŌµÄÓŠŠņÅÅĮŠ£»
D”¢ÓÉÓŚ¾§ĢåŌŚ²»Ķ¬·½ĻņÉĻĪļÖŹĪ¢Į£µÄÅÅĮŠĒéæö²»Ķ¬£¬¼“ĪŖø÷ĻņŅģŠŌ£®
½ā“š ½ā£ŗA”¢·Ö×Ó¾§ĢåČŪ»ÆŹ±Ņ»°ćĘĘ»µ·Ö×Ó¼ä×÷ÓĆĮ¦£¬¶ų²»Ó°Ļģ»Æѧ¼ü£¬Čēµāµ„ÖŹČŪ»Æ£¬¹ŹA“ķĪó£»
B”¢¾§ĢåŌŚ¹ĢĢ¬Ź±²»¾ßÓŠ×Ō·¢ŠŌ£¬Äܹ»×Ō·¢µŲ³ŹĻÖ¹ęŌņµÄ¶ąĆęĢåĶāŠĪ£¬¹ŹBÕżČ·£»
C”¢¹¹³É¾§ĢåµÄĮ£×ÓŌŚĪ¢¹ŪæÕ¼äĄļ³ŹĻÖÖÜĘŚŠŌµÄÓŠŠņÅÅĮŠ£¬¾§ĢåµÄÕāŅ»½į¹¹ĢŲÕ÷æÉŅŌĶعżX-ÉäĻßŃÜÉäĶ¼Ę×·“Ó³³öĄ“£®Ņņ“Ė£¬Ēų·Ö¾§ĢåŗĶ·Ē¾§ĢåµÄ×īæÉææµÄæĘѧ·½·ØŹĒ¶Ō¹ĢĢå½ųŠŠX-ÉäĻßŃÜÉ䏵Ń飬¹ŹCÕżČ·£»
D”¢ÓÉÓŚ¾§ĢåŌŚ²»Ķ¬·½ĻņÉĻĪļÖŹĪ¢Į£µÄÅÅĮŠĒéæö²»Ķ¬£¬¼“ĪŖø÷ĻņŅģŠŌ£¬¾ßÓŠĢŲ¶ØµÄ·½ĻņŠŌ£¬¹ŹDÕżČ·£»
¹ŹŃ”A£®
µćĘĄ ½ā¾ö±¾ĢāŠčÖŖµĄ£ŗµ„¾§Ģåø÷ĻņŅģŠŌ£¬¶ų¶ą¾§Ģåø÷ĻņĶ¬ŠŌ£®×¢Ņā¾§ĢåÓė·Ē¾§ĢåµÄĒų±šŹĒÓŠĪŽ¹Ģ¶ØČŪµć£®


 ŌĶĮæģ³µĻµĮŠ“š°ø
ŌĶĮæģ³µĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 2£ŗ3 | B£® | 3£ŗ2 | C£® | 1£ŗ1 | D£® | 2£ŗ1 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 254 g I2£Øg£©ÖŠĶØČė2 g H2£Øg£©£¬·“Ó¦·ÅČČ9.48 kJ | |
| B£® | 1 mol¹ĢĢ¬µāÓė1 molĘųĢ¬µāĖłŗ¬µÄÄÜĮæĻą²ī17.00 kJ | |
| C£® | ·“Ó¦£Ø¢¢£©µÄ·“Ó¦Īļ×ÜÄÜĮæ±Č·“Ó¦£Ø¢”£©µÄ·“Ó¦Īļ×ÜÄÜĮæµĶ | |
| D£® | ·“Ó¦£Ø¢”£©µÄ²śĪļ±Č·“Ó¦£Ø¢¢£©µÄ²śĪļĪČ¶Ø |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | CO2”¢H2S | B£® | SO3”¢CH4 | C£® | C60”¢C2H4 | D£® | NH3”¢HCl |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
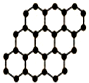 CŗĶSiŌŖĖŲŌŚ»ÆŃ§ÖŠÕ¼ÓŠ¼«ĘäÖŲŅŖµÄµŲĪ»£®
CŗĶSiŌŖĖŲŌŚ»ÆŃ§ÖŠÕ¼ÓŠ¼«ĘäÖŲŅŖµÄµŲĪ»£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | CO2 | B£® | CH3COOHČÜŅŗ | C£® | ŅŅĶé | D£® | Na2CO3ČÜŅŗ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Li”¢Na”¢Kµ„ÖŹµÄČŪµćĖę×ÅŗĖµēŗÉŹżµÄŌö¼Ó¶ų½µµĶ | |
| B£® | µŚ¶žÖÜĘŚŌŖĖŲ“ÓLiµ½F£¬·Ē½šŹōŠŌÖš½„ŌöĒæ | |
| C£® | Ā±×åŌŖĖŲĒā»ÆĪļµÄ·ŠµćĖę×ÅŗĖµēŗÉŹżµÄŌö¼Ó¶ųÉżøß | |
| D£® | ŌŚŌŖĖŲÖÜĘŚ±ķÖŠµŚČż×ŻĮŠŗ¬ÓŠµÄŌŖĖŲÖÖĄą×ī¶ą |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Ö»ÓŠ¢Ł¢Ś¢Ż | B£® | Ö»ÓŠ¢Ł¢Ś¢Ū¢Ü | C£® | Ö»ÓŠ¢Ś¢Ū¢Ż | D£® | Č«²æ |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com