
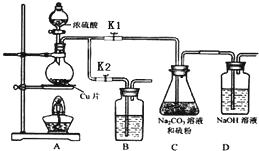
 硫代硫酸钠(Na2S2O3)可由亚硫酸钠和硫粉通过化合反应制得.
硫代硫酸钠(Na2S2O3)可由亚硫酸钠和硫粉通过化合反应制得.| 编号 | 1 | 2 | 3 |
| 溶液的体积/mL | 10.00 | 10.00 | 10.00 |
| 消耗I2标准溶液的体积/mL | 19.95 | 17.10 | 20.05 |
分析 (Ⅰ)①铜和浓硫酸加热反应生成硫酸铜、二氧化硫和水;
②Na2S2O3在酸性溶液中不能稳定存在,二氧化硫通入碳酸钠溶液中反应生成亚硫酸钠和硫粉反应生成硫代硫酸钠;装置D是用氢氧化钠吸收未反应的二氧化硫和产生的二氧化碳;停止C装置反应打开K2,关闭K1;
④装置B是利用氢氧化钠溶液吸收多余的二氧化硫气体;
(Ⅱ)以淀粉溶液为指示剂,用浓度为0.050mol/L I2的标准溶液进行滴定,终点现象为溶液变蓝色且半分钟内不褪色;依据反应的定量关系 2S2O32-+I2→S4O62-+2I-.计算碘单质消耗的硫代硫酸钠,计算得到样品中的质量分数.
解答 解:(Ⅰ)①铜和浓硫酸加热反应生成硫酸铜、二氧化硫和水,反应的化学方程式为:Cu+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O,
故答案为:Cu+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O;
②Na2S2O3在酸性溶液中不能稳定存在,二氧化硫通入碳酸钠溶液中反应生成亚硫酸钠和硫粉反应生成硫代硫酸钠,C中混合液被气流搅动,反应一段时间后,硫粉的量逐渐减少,所以C中碳酸钠的作用是做反应物,提供碱性环境,装置D是用氢氧化钠吸收未反应的二氧化硫和产生的二氧化碳,反应的离子方程式为SO2+2OH -=SO32-+H2O、CO2+2OH -=CO32-+H2O,停止C中的反应的操作是应打开K2,关闭K1 ,
故答案为:提供碱性环境,作反应物;SO2+2OH -=SO32-+H2O、CO2+2OH -=CO32-+H2O;打开K2,关闭K1;
④为防止过量的二氧化硫污染性气体排放到空气中污染环境,装置B是利用氢氧化钠溶液吸收多余的二氧化硫气体;
故答案为:NaOH;在C中的反应停止后,吸收A中产生的多余SO2,防止空气污染;
(Ⅱ)以淀粉溶液为指示剂,用浓度为0.050mol/L I2的标准溶液进行滴定,终点现象为溶液变蓝色且半分钟内不褪色;根据表中数据可知,第二次实验中消耗I2标准溶液的体积偏小,舍去,则实际消耗I2标准溶液的体积的平均值是=$\frac{19.95+20.05}{2}$=20ml,则根据反应的方程式可知,2S2O32-+I2→S4O62-+2I-,所以样品中Na2S2O3•5H2O的物质的量是0.050mol/L×0.0200L×2×10=0.02mol,则Na2S2O3•5H2O在产品中的质量分数=$\frac{0.02mol×248g/mol}{5.5g}$×100%=90.2%;
故答案为:加入最后一滴I2标准溶液后,溶液变蓝,且半分钟内颜色不改变;90.2%.
点评 本题考查了物质性质的实验验证和实验方法应用,物质性质的掌握和实验基本操作是解题关键,题目难度中等.


 冲刺100分1号卷系列答案
冲刺100分1号卷系列答案科目:高中化学 来源: 题型:解答题
 葡萄可用于酿酒.
葡萄可用于酿酒. CH3COOC2H5+H2O.
CH3COOC2H5+H2O.| ①称取E4.5g,升温使其汽化,测其密度是相同条件下H2的45倍. | ①有机物E的相对分子量为90: |
| ②将此9.0gE在足量纯O2充分燃烧,并使其产物依次通过碱石灰、无水硫酸铜粉末、足量石灰水,发现碱石灰增重14.2g,硫酸铜粉末没有变蓝,石灰水中有10.0g白色沉淀生成;向增重的碱石灰中加入足量盐酸后,产生4.48L无色无味气体(标准状况). | ②9.0g有机物E完全燃烧时,经计算:生成CO2共为0.3 mol, 生成的H2O5.4g. 有机物E的分子式C3H6O3 |
| ③经红外光谱测定,证实其中含有羟基,羧基,甲基; | ③E的结构简式CH3CH(OH)COOH |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 有机物在滤液中 | B. | 杂质在滤液中 | C. | 有机物滤纸上 | D. | 杂质在溶剂中 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题


查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| 温度(绝对温度) | K1 | K2 |
| 973 | 1.47 | 2.38 |
| 1173 | 2.15 | 1.67 |
| 时间/min | CO2 | H2 | CO | H2O |
| 0 | 0.2000 | 0.3000 | 0 | 0 |
| 2 | 0.1740 | 0.2740 | 0.0260 | 0.0260 |
| 3 | C1 | C2 | C3 | C3 |
| 4 | C1 | C2 | C3 | C3 |
| 5 | 0.0727 | 0.1727 | 0.1273 | 0.1273 |
| 6 | 0.0350 | 0.1350 | 0.1650 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
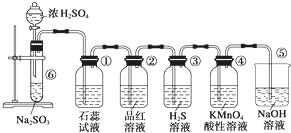 图是实验室制取SO2并验证SO2的某些性质的装置,试回答:
图是实验室制取SO2并验证SO2的某些性质的装置,试回答:查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com