
| A. | c(H+)>c(F-) | B. | c(H+)>c(HF) | C. | c(OH-)<c(HF) | D. | c(HF)>c(F-) |
分析 0.1mol•L-1HF溶液的pH=2,氢离子浓度为0.01mol/L,说明HF为弱酸,在溶液中部分电离,根据物料守恒c(HF)+c(F-)=0.1mol/L可知,c(HF)≈0.09mol/L,结合电荷守恒进行判断.
解答 解:0.1mol•L-1HF溶液的pH=2,氢离子浓度为0.01mol/L,
A.HF溶液中存在电荷守恒:c(H+)=c(OH-)+c(F-),则c(H+)>c(F-),故A正确;
B.该溶液中c(H+)=0.01mol/L,由于水的电离程度较小,则c(H+)≈c(F-),根据物料守恒c(HF)+c(F-)=0.1mol/L可知,c(HF)≈0.09mol/L,所以c(H+)<c(HF),故B错误;
C.HF为酸溶液,溶液中氢氧根离子浓度非常小,则c(OH-)<c(HF),故C正确;
D.根据B可知,c(F-)≈c(H+)=0.01mol/L,c(HF)≈0.09mol/L,则c(HF)>c(F-),故D正确;
故选B.
点评 本题考查了离子浓度大小比较,题目难度不大,明确溶液酸碱性与溶液pH的关系为解答关键,注意掌握电荷守恒、物料守恒的含义及应用方法,试题培养了学生的分析、理解能力.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 稀品红溶液 | B. | Ca(OH)2溶液 | C. | 溴水 | D. | 饱和H2S溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
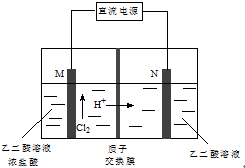 乙醛酸(HOOC-CHO)是有机合成的重要中间体.工业上用“双极室成对电解法”生产乙醛酸,原理如图所示.该装置中阴、阳两极为惰性电极,两极室均可产生乙醛酸,其中乙二醛与M电极的产物反应生成乙醛酸.下列说法正确的是( )
乙醛酸(HOOC-CHO)是有机合成的重要中间体.工业上用“双极室成对电解法”生产乙醛酸,原理如图所示.该装置中阴、阳两极为惰性电极,两极室均可产生乙醛酸,其中乙二醛与M电极的产物反应生成乙醛酸.下列说法正确的是( )| A. | M极与直流电源的负极相连 | |
| B. | 若有2 molH+通过质子交换膜并完全参与反应,则该装置中生成的乙醛酸为1 mol | |
| C. | N电极上的电极反应式:HOOC-COOH-2e-+2H+=HOOC-CHO+H2O | |
| D. | 乙二醛与M电极的产物反应生成乙醛酸的化学方程式:Cl2+OHC-CHO+H2O=HOOC-CHO+2HCl |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
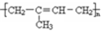 )为主要成分的天然高分子化合物.天然橡胶有两种,一种是巴西三叶橡胶树产出的橡胶,通常就称为天然橡胶;另一种是杜仲树产出的橡胶,它是我国特产,在湖北等地都有大面积种植,被称为杜仲胶.
)为主要成分的天然高分子化合物.天然橡胶有两种,一种是巴西三叶橡胶树产出的橡胶,通常就称为天然橡胶;另一种是杜仲树产出的橡胶,它是我国特产,在湖北等地都有大面积种植,被称为杜仲胶.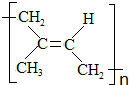 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na+、Fe2+、Cl-、SO42- | B. | K+、[Al(OH)4]-、Cl-、SO42- | ||
| C. | Ca2+、Mg2+、NO3-、HCO${\;}_{3}^{-}$ | D. | Na+、Cl-、CO32-、SO32- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com