
【题目】下列离子方程式正确的是
A. 锌与稀硝酸反应: Zn+2H+===Zn2++H2↑
B. Al2O3与少量NaOH溶液反应:Al3++3OH- =Al(OH)3↓
C. 碳酸氢钠溶液与氢氧化钠溶液反应:H++OH-=H2O
D. 向偏铝酸钠溶液中通入过量CO2:AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】甲、乙两化学活动小组对中学化学教材中“氨的催化氧化”进行了实验探究。
(1)甲小组设计了如图l所示的实验装置(固定装置已略去)。
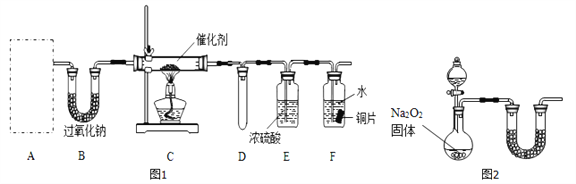
①若装置A中使用的药品是NH4HCO3固体,则A需要的仪器有试管、导管、橡胶塞和_____(填选项序号)。
a.锥形瓶 b.酒精灯 c.烧瓶 d.蒸发皿
②装置B的作用是______________;装置D的作用是____________。
③装置C中发生反应的化学方程式为_________________。
④若A、B中药品足量,则可以观察到装置F中的实验现象是_______________。
⑤该装置存在的主要缺陷是____________________。
(2)乙小组认为可将甲小组的装置中A、B部分换成如图2所示装置(其余部分相同)进行实验。
①烧瓶中加入的是过氧化钠固体,则分液漏斗中加入的最佳试剂是______,U型管中加入试剂是______。
②实验室制备氨气的化学反应方程式是________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工厂中用稀硫酸浸泡某矿石后的溶液中,除了含有大量硫酸外,还含有少量NH![]() 、Fe3+、AsO
、Fe3+、AsO![]() 、Cl-。为除去杂质离子,部分操作流程如下:
、Cl-。为除去杂质离子,部分操作流程如下:
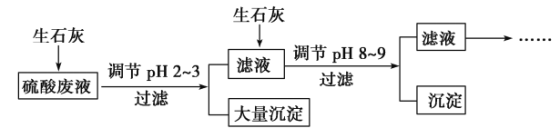
请回答问题:
(1)用稀硫酸浸泡某矿石后的溶液中,硫酸的浓度为4.9 g·L-1,则该溶液中的pH约为_____________________________。
(2)NH![]() 在用稀硫酸浸泡某矿石后的溶液中以(NH4)2SO4和NH4Cl形式存在。现有一份(NH4)2SO4溶液,一份NH4Cl溶液,(NH4)2SO4溶液中c(NH
在用稀硫酸浸泡某矿石后的溶液中以(NH4)2SO4和NH4Cl形式存在。现有一份(NH4)2SO4溶液,一份NH4Cl溶液,(NH4)2SO4溶液中c(NH![]() )恰好是NH4Cl溶液中c(NH
)恰好是NH4Cl溶液中c(NH![]() )的2倍,则c[(NH4)2SO4]__________c(NH4Cl)(填“<”“=”或“>”)。
)的2倍,则c[(NH4)2SO4]__________c(NH4Cl)(填“<”“=”或“>”)。
(3)随着向废液中投入生石灰(忽略溶液温度的变化),溶液中![]() __________(填“增大”“减小”或“不变”)。
__________(填“增大”“减小”或“不变”)。
(4)投入生石灰调节pH到2~3时,大量沉淀主要成分为CaSO4·2H2O[含有少量Fe(OH)3],提纯CaSO4·2H2O的主要操作步骤:向沉淀中加入过量________,充分反应后,过滤、洗涤、__________________________。
(5)25 ℃,H3AsO4电离常数为K1=5.6×10-3,K2=1.7×10-7,K3=4.0×10-12。当溶液中pH调节到8~9时,沉淀主要成分为Ca3(AsO4)2。
①pH调节到8左右Ca3(AsO4)2才开始沉淀的原因是_____________________。
②Na3AsO4第一步水解的平衡常数数值为___________________。
③已知:AsO![]() +2I-+2H+===AsO
+2I-+2H+===AsO![]() +I2+H2O,SO2+I2+2H2O===SO
+I2+H2O,SO2+I2+2H2O===SO![]() +2I-+4H+。上述两个反应中还原性最强的微粒是__________。
+2I-+4H+。上述两个反应中还原性最强的微粒是__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向MgSO4和Al2(SO4)3的混合溶液中, 逐滴加入NaOH溶液。下列图象中(横坐标表示NaOH溶液的体积, 纵坐标表示沉淀质量), 能正确表示上述反应的是 ( )

A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳酸氢铵是我国主要的氮肥品种之一,在贮存和运输过程中容易挥发损失。为了鉴定其质量和确定田间施用量,必须测定其含氮量。
Ⅰ.某学生设计了一套以测定二氧化碳含量间接测定含氮量的方法。将样品放入圆底烧瓶中:
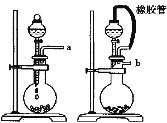
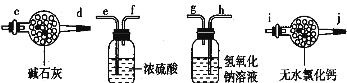
(1)请选择必要地装置,按气流方向连接顺序为 。
(2)分液漏斗中的液体最适合的是 。
A.稀盐酸 B.稀硫酸 C.浓硝酸 D.氢氧化钠
(3)连在最后的装置起到的作用 。
Ⅱ.如果氮肥中成分是(NH4)2SO4,则可以用甲醛法测定含氮量。甲醛法是基于甲醛与一定量的铵盐作用,生成相当量的酸,反应为2(NH4)2SO4+6HCHO=(CH2)6N4 +2H2SO4 + 6H2O,生成的酸再用氢氧化钠标准溶液滴定,从而测定氮的含量。步骤如下:
(4)用差量法称取固体(NH4)2SO4样品0.6g于烧杯中,加入约30mL蒸馏水溶解,最终配成100mL溶液。用 (填“酸式”或“碱式”)滴定管准确取出20.00mL的溶液于锥形瓶中,加入18%中性甲醛溶液5mL,放置5min后,加入1~2滴 指示剂(已知滴定终点的pH约为8.8),用浓度为0.08mol/L氢氧化钠标准溶液滴定,读数如下表:
滴定次数 | 滴定前读数(mL) | 滴定后读数(mL) |
1 | 1.20 | 16.21 |
2 | 3.00 | 18.90 |
3 | 4.50 | 19.49 |
达滴定终点时的现象为 ,由此可计算出该样品中的氮的质量分数为 。
(5)在滴定实验结束后发现滴定用的碱式滴定管玻璃尖嘴内出现了气泡,滴定开始时无气泡,则此实验测定的含氮量比实际值 (填“偏大”“偏小”或“无影响”)。
Ⅲ.如果测定碳酸氢铵中的含氮量时,使用甲醛法是否合理 (填“是”或“否”),理由是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学生的实验报告所列出的下列数据中合理的是( )
A.用10mL量筒量取 7.13 mL稀盐酸
B.用托盘天平称量 25.20gNaCl
C.用广泛pH试纸测得某溶液的pH为 2.3
D.用25 mL滴定管做中和滴定时,用去某浓度的碱溶液 21.70 mL
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com