
(12��)��֪�����������ڡ���������Ķ����ڷǽ���Ԫ��X��Y��������������ˮ�����Ϊǿ�ᡣ������ͼת����ϵ(��Ӧ���������ֲ�������ȥ)���ش��������⣺
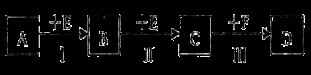
��1����A��B��C��D��Ϊ��XԪ�صĻ������A��F�ķ��Ӿ�Ϊ10����������
��F����____________(����ӻ�������ۻ����)��
�ڷ�ӦI�Ļ�ѧ����ʽΪ____________________________________________��
�۽�1.92gͭ����һ������D��Ũ��Һ��Ӧ����ͭ����ȫ��Ӧʱ�ռ�������1.12L(��״��)����Ӧ���ĵ�D�����ʵ���Ϊ________________mol��
��2����A��B��C��D��Ϊ��YԪ�صĻ��������A������Ԫ����ɣ���A��Ħ������Ϊ34 g/mol����
�ٽ�ͭ����D��Ũ��Һ��Ӧ������Һ�������ɣ��õ��İ�ɫ��������Ϊ____________(�ѧʽ)��
�ڽ��پ�Na2Y��Һ�μӵ�����������Һ�з�����Ӧ���������ɣ���д���÷�Ӧ�����ӷ�Ӧ����ʽ__________���ڸ÷�Ӧ������74.5 g NaClO����ԭ����ת�Ƶ��ӵ����ʵ���Ϊ_________mol��
��12�֣�ÿ��2�֣���1���ٹ��ۻ����� ;�� 4NH3��5O2 4NO��6H2O ;�� 0.11 ��
4NO��6H2O ;�� 0.11 ��
��2����CuSO4 ; �� S2����4ClO��===SO42����4Cl�� ��2 ��
��������
�����������1���������⣬��A��B��C��D��Ϊ��XԪ�صĻ������A��F�ķ��Ӿ�Ϊ10����������A��NH3��B��NO��C��NO2��D��HNO3��E��O2��F��H2O����F��H2O���ۻ�����ڷ�ӦI�Ļ�ѧ����ʽΪ4NH3��5O2 4NO��6H2O����n(Cu)=1.92g��64g/mol=0.03mol����Ӧ��ʼʱ������ӦCu+4HNO3(Ũ)=Cu(NO3)2+NO2��+2H2O������Һ��ϡ������Ӧ��3Cu��8HNO3(ϡ)=2Cu(NO3)2��2NO����4H2O ������n(NO2)+n(NO) = 1.12L��22.4L/mol=0.05mol����Ӧ���ĵ����������������������Ϊ�������������ñ�ΪCu(NO3)2����n(HNO3)=2n(Cu)+n(����)=0.03mol��2+0.05mol=0.11mol����2����A��B��C��D��Ϊ��YԪ�صĻ��������A������Ԫ����ɣ���A��Ħ������Ϊ34g/mol����A��H2S��B��SO2��C��SO3��D��H2SO4��E��O2��F��H2O. �ٽ�ͭ����D��Ũ��Һ���ȣ�������ӦCu��2H2SO4(Ũ)
4NO��6H2O����n(Cu)=1.92g��64g/mol=0.03mol����Ӧ��ʼʱ������ӦCu+4HNO3(Ũ)=Cu(NO3)2+NO2��+2H2O������Һ��ϡ������Ӧ��3Cu��8HNO3(ϡ)=2Cu(NO3)2��2NO����4H2O ������n(NO2)+n(NO) = 1.12L��22.4L/mol=0.05mol����Ӧ���ĵ����������������������Ϊ�������������ñ�ΪCu(NO3)2����n(HNO3)=2n(Cu)+n(����)=0.03mol��2+0.05mol=0.11mol����2����A��B��C��D��Ϊ��YԪ�صĻ��������A������Ԫ����ɣ���A��Ħ������Ϊ34g/mol����A��H2S��B��SO2��C��SO3��D��H2SO4��E��O2��F��H2O. �ٽ�ͭ����D��Ũ��Һ���ȣ�������ӦCu��2H2SO4(Ũ)  CuSO4��SO2����2H2O��������Һ�������ɣ��õ��İ�ɫ��������ΪCuSO4���ڽ��پ�Na2Y��Һ�μӵ�����������Һ�з�����Ӧ���������ɣ����ݵ����غ㡢����غ㼰ԭ���غ�ɵø÷�Ӧ�����ӷ�Ӧ����ʽS2����4ClO��===SO42����4Cl����n(NaClO)=74.5 g ��74.5 g/mol=1mol�����ݷ���ʽ��֪��ÿ��4mol��NaClO ������Ӧ��ת�Ƶ��ӵ����ʵ�����8mol������NaClO �����ʵ�����1mol������ת�Ƶ��ӵ����ʵ�����2mol��
CuSO4��SO2����2H2O��������Һ�������ɣ��õ��İ�ɫ��������ΪCuSO4���ڽ��پ�Na2Y��Һ�μӵ�����������Һ�з�����Ӧ���������ɣ����ݵ����غ㡢����غ㼰ԭ���غ�ɵø÷�Ӧ�����ӷ�Ӧ����ʽS2����4ClO��===SO42����4Cl����n(NaClO)=74.5 g ��74.5 g/mol=1mol�����ݷ���ʽ��֪��ÿ��4mol��NaClO ������Ӧ��ת�Ƶ��ӵ����ʵ�����8mol������NaClO �����ʵ�����1mol������ת�Ƶ��ӵ����ʵ�����2mol��
���㣺����Ԫ�ؼ���������ƶϡ���ѧ��Ӧ����ʽ����д��������ԭ��Ӧ�еĵ���ת�Ƽ��غ㷽����������ԭ��Ӧ�ļ����е�Ӧ�õ�֪ʶ��


 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�긣��ʡ������ѧ�ڵ��Ĵ��¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
��ҵ�������������ʣ����漰������ԭ��Ӧ����
A��������������Ҫ�ɷ�Al2O3������������
B������������Ҫ�ɷ�FeS2����������
C���ú�ˮ�����������Ȼ�þ����
D�����Ȼ��������ռ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ���㽭ʡ������ѧ��10���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
�������ӷ���ʽ��д��ȷ����
A�����Ȼ�������Һ��ϡ�����ϣ�Fe2++4H++NO3-=Fe3++2H2O+NO��
B����NH4HSO4ϡ��Һ����μ���Ba(OH)2ϡ��Һ��SO42-�պó�����ȫ��Ba2+ + 2OH- + NH4+ + H+ + SO4 2- = BaSO4��+ NH3��H2O + H2O
C��Ư����Һ��ͨ������SO2���壺Ca2+ +2ClO- +SO2 +H2O =CaSO3��+2HClO
D��Fe(OH)3��������HI��Һ��Ӧ: Fe(OH)3+3H+=Fe3++3H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ���Ĵ�ʡ�����и���һ��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
��֪�ס��ҡ����������ʾ�����ͬһ����ѧ����Ԫ��X����ת����ϵ���£�
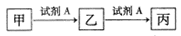
����˵������ȷ����
A������ΪNaHCO3�����һ����CO2
B����AΪ��ˮ��XΪ����Ԫ�أ���������Ӧ��������
C����AΪNaOH��Һ��XΪ�����ڵĽ���Ԫ�أ�����һ��Ϊ��ɫ����
D������Ϊ�������������ˮ�γɵ�Ũ��Һ����̼��Ӧ��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ���Ĵ�ʡ�����и���һ��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
���й��ڻ�ѧ����ı�ʾ��ȷ����
A���⻯淋ĵ���ʽ��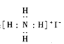
B������ױ��Ľṹ��ʽ��
C��������Ϊ146��������Ϊ92����(u)ԭ�ӣ�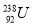
D����ԭ�ӵĽṹʾ��ͼ�� 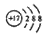
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ��ɽ��ʡ�����и���12��У�����ϼ�⻯ѧ�Ծ��������棩 ���ͣ�ѡ����
����˵����ȷ����
A���к͵�����������ʵ���Ũ�ȵ�����ʹ��������ĵ�NaOH�����ʵ������
B����NaHA��Һ��pH<7����H2Aһ����ǿ��
C����NaOH��Һ���뵽NH4Cl��Һ������ʱ����Һ��c(NH4+)=c(Clһ)
D�������£���pH=11��Ba(OH)2��Һ��ˮϡ��10������Һ��pH=12
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ��ɽ��ʡ�����и���12��У�����ϼ�⻯ѧ�Ծ��������棩 ���ͣ�ѡ����
�����£����и���������ָ����Һ��һ���ܴ����������
A��c(H+)<c(OH-)����Һ�У�Na+��K+��SO42-��ClOһ
B����ʹ��̪������Һ�У�Na+��Cu2+��CO32-��NO3һ
C��0.1 mol/LFeCl3��Һ�У�K+��NH4+��Iһ��SCN��
D�����������ܲ�����������Һ�У�NH4+��Fe2+��NO3-��SO42-
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�����ʡӢ��ѧУ������ѧ��12���¿���ѧ�Ծ��������棩 ���ͣ������
��9�֣��������ƣ�NaClO2����һ��ǿ������Ư�����㷺���ڷ�֯��ӡȾ��ʳƷ��ҵ�����ڼ��Ի������ȶ����ڡ�ijͬѧ�������Ϻ��������NaClO2����Ҫ�������¡�
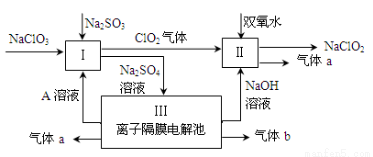
��1�����з�����Ӧ�Ļ�ԭ���ֱ��� �� ���ѧʽ����
��2�����з�Ӧ�����ӷ���ʽ�� ��
��3��A�Ļ�ѧʽ�� ��װ�â���A�� ����������
��4��ClO2��һ�ָ�Чˮ�������������������ƺ�ϡ����Ϊԭ���Ʊ���д�����Ʊ���Ӧ�Ļ�ѧ����ʽ ��
��5��NaClO2���ʿɷֽ�ΪNaClO3��NaCl��ȡ����������ǰ���NaClO2�����������Һ���ֱ�������FeSO4��Һ��Ӧʱ������Fe2+�����ʵ��� �������ͬ��������ͬ�������жϡ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�긣��ʡ������ѧ��12���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
�����ʵ�����Ϊ0.1 mol��AlCl3��CuCl2��H2SO4����ˮ�Ƴ�100 mL�Ļ����Һ,��ʯī���缫���,���ռ����缫������������,һ��ʱ����������ռ�������������ͬ�����������ͬ��������������ȷ����
A�������õ�����������O2��Ϊ0.35 mol
B����Ԫ�ؽ���Al(OH)3����ʽ����
C��������������3.2 g
D����·�й�ת��0.9 mol����
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com