
| A. | 原电池是将电能转变为化学能的装置 | |
| B. | 负极发生的反应为:Fe-2e-=Fe 2+ | |
| C. | 正极发生的反应为:2H2O+O2+2e-=4OH- | |
| D. | 钢柱在水下的部分比在空气和水交界出更容易腐蚀 |
分析 钢铁在潮湿的空气中会被腐蚀,发生的原电池反应为:2Fe+2H2O+O2=2Fe(OH)2是发生的吸氧腐蚀,原电池中负极Fe发生氧化反应,反应式为Fe-2e-Fe2+,正极氧气发生还原反应,反应式为O2+2H2O+4e-═4OH-,据此分析.
解答 解:钢铁中含有铁和碳,在潮湿的环境中构成原电池,铁作负极,碳作正极.
A、原电池是化学能转化为电能的装置,故A错误;
B、根据反应方程式知,负极反应式为Fe-2e-Fe2+,故B正确;
C、根据反应方程式知,正极反应式为O2+2H2O+4e-═4OH-,故C错误;
D、氧气在水中的溶解度较小,在空气与水交界处更易接触氧气,在水下部分比在空气与水交界处更难腐蚀,故D错误.
故选B.
点评 本题考查了原电池正、负极的判断,基础是氧化还原反应,可以直接根据化合价的升降来判断正负极.发生氧化反应的一极为负极,发生还原反应的一极为正极,题目较简单.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 单位体积内活化分子数增多 | B. | 活化分子百分含量增多 | ||
| C. | 单位体积内活化分子数不变 | D. | 活化分子百分含量减少 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | KI溶液在空气久置变黄:4I-+O2+4H+=2I2+2H2O | |
| B. | 用稀盐酸除去久存石灰水的烧杯内壁上的固体:2H++Ca(OH)2=Ca2++2H2O | |
| C. | 用酸性KMnO4溶液除去CO2中SO2:3SO2+2MnO4-+4H+=3SO42-+2MnO2↓+H2O | |
| D. | 用足量饱和Na2CO3溶液吸收制备的乙酸乙酯:CO32-+CH3COOH=HCO3-+CH3COO- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1molH3PO4的质量为98g•mol-1 | B. | H3PO4的摩尔质量为98g | ||
| C. | 9.8g H3PO4含有NA个H3PO4分子 | D. | NA个H3PO4分子的质量为98g |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 化学变化的同时总伴随着能量变化 | |
| B. | 需加热才反应的一定是吸热反应 | |
| C. | 在常温下就能进行的反应一定是放热反应 | |
| D. | 反应物的总能量大于生成物的总能量的反应是吸热反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
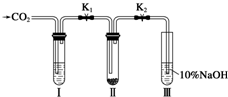 某课题研究小组的同学在查阅资料时得知,Na2O2与干燥的CO2不能发生反应,当有少量水存在时,Na2O2可与CO2发生反应生成Na2CO3和O2.为了探究“二氧化碳是否在有水存在时才能与过氧化钠反应”.某课题研究小组的同学们设计了如图所示的实验装置,分别进行甲、乙两次实验:
某课题研究小组的同学在查阅资料时得知,Na2O2与干燥的CO2不能发生反应,当有少量水存在时,Na2O2可与CO2发生反应生成Na2CO3和O2.为了探究“二氧化碳是否在有水存在时才能与过氧化钠反应”.某课题研究小组的同学们设计了如图所示的实验装置,分别进行甲、乙两次实验:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 体积不变,增加H2O(g)的量 | |
| B. | 保持体积不变,充入Ne使体系压强增大 | |
| C. | 将容器的体积缩小一半 | |
| D. | 压强不变,充入He使容器的体积增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,11.2L四氯化碳所含分子数为0.5 NA | |
| B. | 1mol/L的盐酸溶液中,所含氯化氢分子数为NA | |
| C. | 80g硝酸铵含有氮原予数为2NA | |
| D. | 1mol氯气和铁反应时转移的电子数为3NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com