
【题目】一定温度下,在三个容积相同的恒容密闭容器中按不同方式投入反应物,发生反应2SO2(g)+O2(g)![]() 2SO3(g)(正反应放热),测得反应的相关数据如下:
2SO3(g)(正反应放热),测得反应的相关数据如下:
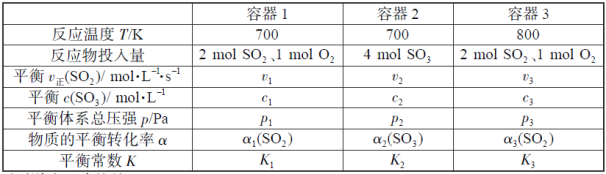
下列说法正确的是
A.v1<v2,c2<2c1B.K1>K3,p2>2p3
C.v1<v3,α1(SO2)<α3(SO2)D.c2>2c3,α2(SO3)+α3(SO2)<1
【答案】D
【解析】
针对反应2SO2(g)+O2(g)![]() 2SO3(g)(正反应放热),容器2中加入4mol SO3,等效于在相同温度、相同容积下反应物投入量为4mol SO2、2mol O2,为容器1投入量的两倍,则容器2可看作是先由两个容器1达到平衡后再压缩到容器1的体积,增大压强反应速率加快,有v1<v2,增大压强,若平衡不移动,c2=2c1,p2=2p1,对于该反应,增大压强平衡向着正方向移动,则平衡时c2>2c1,p2<2p1,α1(SO2)+α2(SO3)<1,容器1和2的温度相同,则K1=K2;
2SO3(g)(正反应放热),容器2中加入4mol SO3,等效于在相同温度、相同容积下反应物投入量为4mol SO2、2mol O2,为容器1投入量的两倍,则容器2可看作是先由两个容器1达到平衡后再压缩到容器1的体积,增大压强反应速率加快,有v1<v2,增大压强,若平衡不移动,c2=2c1,p2=2p1,对于该反应,增大压强平衡向着正方向移动,则平衡时c2>2c1,p2<2p1,α1(SO2)+α2(SO3)<1,容器1和2的温度相同,则K1=K2;
容器3的投入量与容器1相同,温度比容器1高,可以看做是容器1达到平衡后升高温度的新平衡,升高温度反应速率加快,则v1<v3,对于该反应,升高温度平衡逆向移动,则c3<c1,p3>p1,a1(SO2)>a3(SO2),K1>K3,据此分析作答。
针对反应2SO2(g)+O2(g)![]() 2SO3(g)(正反应放热),容器2中加入4molSO3,等效于在相同温度、相同容积下反应物投入量为4molSO2、2molO2,为容器1投入量的两倍,则容器2可看作是先由两个容器1达到平衡后再压缩到容器1的体积,增大压强反应速率加快,有v1<v2,增大压强,若平衡不移动,c2=2c1,p2=2p1,对于该反应,增大压强平衡向着正方向移动,则平衡时c2>2c1,p2<2p1,α1(SO2)+α2(SO3)<1,容器1和2的温度相同,则K1=K2;
2SO3(g)(正反应放热),容器2中加入4molSO3,等效于在相同温度、相同容积下反应物投入量为4molSO2、2molO2,为容器1投入量的两倍,则容器2可看作是先由两个容器1达到平衡后再压缩到容器1的体积,增大压强反应速率加快,有v1<v2,增大压强,若平衡不移动,c2=2c1,p2=2p1,对于该反应,增大压强平衡向着正方向移动,则平衡时c2>2c1,p2<2p1,α1(SO2)+α2(SO3)<1,容器1和2的温度相同,则K1=K2;
容器3的投入量与容器1相同,温度比容器1高,可以看做是容器1达到平衡后升高温度的新平衡,升高温度反应速率加快,则v1<v3,对于该反应,升高温度平衡逆向移动,则c3<c1,p3>p1,a1(SO2)>a3(SO2),K1>K3,
A. 容器2等效于两个容器1达到平衡后再压缩到容器1的体积达到的平衡,增大压强反应速率加快,有v1<v2,增大压强,若平衡不移动,c2=2c1,对于该反应,增大压强平衡向着正方向移动,则平衡时c2>2c1,,A项错误;
B. 该反应为放热反应,升高温度,平衡逆向移动,则K1>K3,根据分析,p2<2p1,p3>p1,则p2<2p3,B项错误;
C. 容器3看做是容器1达到平衡后升高温度的新平衡,升高温度反应速率加快,则v1<v3,对于该反应,升高温度平衡逆向移动,α1(SO2)>α3(SO2),C项错误;
D. 根据分析,c2>2c1,c3<c1,则c2>2c3,根据分析,α1(SO2)+α2(SO3)<1,a1(SO2)>a3(SO2),则α2(SO3)+α3(SO2)<1,D项正确;
答案选D。


 名校通行证有效作业系列答案
名校通行证有效作业系列答案科目:高中化学 来源: 题型:
【题目】乙苯和二氧化碳反应生成苯乙烯的过程如图所示。下列说法不正确的是(NA为阿伏加德罗常数的值)( )
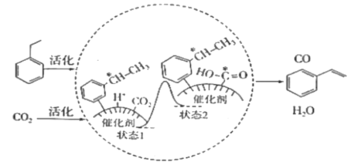
A.10.6g乙苯中所含的极性共价键数目为1.0NA
B.增加二氧化碳的浓度,可能提高苯乙烯的产率
C.状态1到状态2有氧氢键形成
D.标准状况下,10.4g苯乙烯中所含的电子数目为4.0NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“套管实验”是将一个较小的玻璃仪器装入另外一个玻璃仪器中,经组装来完成原来需要两只或更多普通玻璃仪器进行的实验。因其具有许多优点,近年被广泛开发并应用于化学实验中。下述实验为“套管实验”,请观察如图所示实验装置,分析实验原理,回答下列问题:
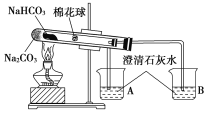
(小试管内塞有沾有无水硫酸铜粉末的棉花球)
(1)从点燃酒精灯开始,试管及烧杯B中能观察到的现象有____________________。
(2)通过该实验可得出的结论是_________________________________。
(3)本装置的优点是_______________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列解释事实或实验现象的化学用语正确的是
A. 硫酸酸化的KI淀粉溶液久置后变蓝:4I-+O2 + 4H+ ![]() 2I2+2H2O
2I2+2H2O
B. 铁和稀硝酸反应制得浅绿色溶液:Fe + 4H+ + NO3-![]() Fe3+ + NO↑+ 2H2O
Fe3+ + NO↑+ 2H2O
C. 水垢上滴入CH3COOH溶液有气泡产生:CaCO3+2H+ ![]() Ca2++CO2↑+ H2O
Ca2++CO2↑+ H2O
D. SO2通入漂白粉溶液中产生白色浑浊:SO2+Ca2++2ClO-+H2O ![]() CaSO3↓+2HClO
CaSO3↓+2HClO
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,向盛有25mLpH=12的一元碱MOH溶液的绝热容器中滴加0.05mol·L-1H2SO4溶液,加入H2SO4溶液的体积(V)与所得混合溶液温度(T)的关系如图所示。下列说法正确的是( )
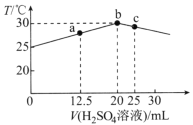
A.应选用酚酞作指示剂
B.a点溶液中存在:c(MOH)+c(M+)<4c(SO![]() )
)
C.水的电离程度:a<b<c
D.b→c的过程中,温度降低的主要原因是溶液中发生了吸热反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁、铬、锰统称为黑色金属,它们的单质、合金及其化合物在科研和生产中有着重要用途。
请回答下列问题:
(1)基态铁原子的价电子轨道表示式为__。铁、铬、锰属于周期表中的___区元素。
(2)基态铬原子和基态锰原子中第一电离能较大的是___(填元素符号),原因为___。
(3)化学式为CrC13·6H2O的化合物有三种结构,一种呈紫罗兰色,一种呈暗绿色,一种呈亮绿色,已知Cr3+的配位数均为6,将它们配制成等体积等浓度的溶液,分别加入足量AgNO3溶液,所得AgC1沉淀的物质的量之比为3:2:1。
①呈暗绿色的配合物内界的化学式为___。
②H2O分子的VSEPR模型为___。
(4)MnF2和MnCl2均为离子化合物,MnF2的熔点高于MnCl2熔点的原因为___。
(5)一氧化锰在医药、冶炼上用途广泛,其立方晶胞结构如图所示。
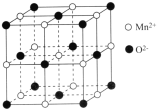
①该晶胞中由O2-形成的正八面体空隙数目为__。
②设NA为阿伏加德罗常数的值,晶胞中距离最近的两个O2-之间的距离为apm,则MnO晶体的密度ρ=____g·cm-3。(用含a、NA的代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】囧烷(G)是一种重要的烃,一种合成囧烷的路线如图所示:
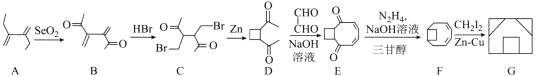
已知: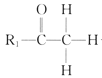 +R2—CHO
+R2—CHO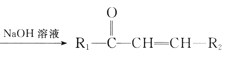 +H2O。
+H2O。
请回答下列问题:
(1)A的化学名称为___;G的分子式为__。
(2)B→C的反应类型为___;C中所含官能团的名称为__。
(3)D→E的化学方程式为___。
(4)同时满足下列条件的B的同分异构体有__种(不考虑立体异构);其中核磁共振氢谱有5组峰的结构简式为___。
①属于芳香族化合物且苯环上连有3个取代基。
②与FeC13溶液发生显色反应。
(5)参照上述合成路线和信息,以![]() 为原料(其他试剂任选),设计制备
为原料(其他试剂任选),设计制备![]() 的合成路线:___。
的合成路线:___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学设计实验探究工业制乙烯的原理和乙烯的主要化学性质,实验装置如图所示(已知烃类都不与碱反应)。请回答下列问题:

(1)工业制乙烯的实验原理是烷烃(液态)在催化剂和加热条件下发生反应生成不饱和烃。例如,石油分馏产物之一的十六烷烃发生反应:C16H34![]() C8H18+甲,甲
C8H18+甲,甲![]() 4乙,则甲的分子式为________,乙的结构简式为____________________________________。
4乙,则甲的分子式为________,乙的结构简式为____________________________________。
(2)B装置中的实验现象可能是________,写出反应的化学方程式:__________,其反应类型是________。
(3)C装置中可观察到的现象是____________,反应类型是________。
(4)查阅资料知,乙烯与酸性高锰酸钾溶液反应产生二氧化碳。根据本实验中装置_____(填字母)中的实验现象可判断该资料是否真实。为了探究溴与乙烯反应是加成反应而不是取代反应,可以测定装置B中溶液在反应前后的酸碱性,简述其理由: __________________。
(5)通过上述实验探究,检验甲烷和乙烯的方法是________(选填字母,下同);除去甲烷中乙烯的方法是________。
A.气体通入水中 B.气体通过盛溴水的洗气瓶
C.气体通过盛酸性高锰酸钾溶液的洗气瓶 D.气体通过氢氧化钠溶液
(6)分别燃烧乙烯和甲烷,甲烷火焰明亮而乙烯产生少量黑烟,原因是_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,在2 L的密闭容器中,加入1mol X(g)和2 mol Y(g)发生反应:X(g)+mY(g)![]() 3Z(g) ΔH<0,平衡时,X和Y的转化率都是10%。下列叙述不正确的是
3Z(g) ΔH<0,平衡时,X和Y的转化率都是10%。下列叙述不正确的是
A.m=2
B.达平衡时,Z的体积分数为10%
C.达平衡后,保持容器体积不变,加热,容器内压强将增大
D.将平衡后的容器体积压缩至1L,X的浓度为0.45mol·L-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com