
| A、在101Kpa时,2gH2完全燃烧生成液态水,放出285.8KJ热量,氢气燃烧的热化学方程式为:2H2(g)+O2(g)=2H2O(l)△H=+285.8KJ/mol |
| B、已知C(石墨,s)C(金刚石,s)△H>0,则石墨比金刚石稳定 |
| C、在稀溶液中H+(aq)+OH-(aq) H2O(l)△H=-57.2 kJ/mol,若将含0.5 mol H2SO4的浓硫酸与含1 mol NaOH的稀溶液混合,放出的热量等于57.2 kJ |
| D、己知2H2(g)+O2(g)2H2O(l)△H1,2H2(g)+O2(g)2H2O(g)△H2,则△H1>△H2 |


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
| A、a>b>c>d |
| B、a>c>b>d |
| C、a>c>d>b |
| D、b>d>c>a |
查看答案和解析>>
科目:高中化学 来源: 题型:
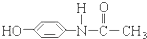 它可能具有的化学性质是( )
它可能具有的化学性质是( )| A、不与烧碱溶液反应 |
| B、能与溴水发生取代反应 |
| C、不能被氧化 |
| D、遇FeCl3溶液发生显色反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、聚丙烯的分子长链是由C-C键连接而成的 |
| B、聚丙烯分子的长链上有支链 |
| C、聚丙烯每个链节内含3个碳原子 |
| D、聚丙烯能使溴水褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、△H<0且熵增大的反应一定可以自发进行 |
| B、△H>0且熵减小的反应一定不能自发进行 |
| C、△H>0且熵增大的反应一定可以自发进行 |
| D、△H<0且熵减小的反应有可能可以自发进行 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、VD=0.01 mol?(L?s)-1 |
| B、VB=0.6 mol?(L?min)-1 |
| C、VC=0.4 mol?(L?min)-1 |
| D、VA=0.15mol?(L?min)-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、X>Y>Z |
| B、Y>Z>X |
| C、X>Z>Y |
| D、Y>X>Z |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com