
【题目】依据A~E几种烃分子的示意图填空。

(1)A分子的空间构型为___________。
(2)B的名称是___________。
(3)D的分子式是___________。
(4)C、E的关系是___________(填“同系物”或“同分异构体”或“同一种物质”)。
(5)A~E表示的物质中,能发生加成反应的两种物质是___________(填序号)。
 提分百分百检测卷系列答案
提分百分百检测卷系列答案 宝贝计划期末冲刺夺100分系列答案
宝贝计划期末冲刺夺100分系列答案 能考试全能100分系列答案
能考试全能100分系列答案科目:高中化学 来源: 题型:
【题目】(1)工业制硝酸的主要反应为4NH3(g)+5O2(g) ![]() 4NO(g)+6H2O(g) ΔH;在容积固定的密闭容器中发生上述反应,容器内部分物质的物质的量浓度如下表:
4NO(g)+6H2O(g) ΔH;在容积固定的密闭容器中发生上述反应,容器内部分物质的物质的量浓度如下表:
浓度 时间 | c(NH3) (mol/L) | c(O2) (mol/L) | c(NO) (mol/L) |
起始 | 0.8 | 1.6 | 0 |
第2 min | 0.6 | a | 0.2 |
第4 min | 0.3 | 0.975 | 0.5 |
第6 min | 0.3 | 0.975 | 0.5 |
第8 min | 0.7 | 1.475 | 0.1 |
①反应在第2 min到第4 min时,O2的平均反应速率为________。
②反应在第6 min时改变了条件,改变的条件可能是________(填序号)。
A.使用催化剂 B.升高温度 C.减小压强 D.增加O2的浓度
③下列说法中能说明4NH3(g)+5O2(g)![]() 4NO(g)+6H2O(g)达到平衡状态的是________(填序号)。
4NO(g)+6H2O(g)达到平衡状态的是________(填序号)。
A.单位时间内生成n mol NO的同时,反应n mol NH3
B.条件一定,混合气体的平均相对分子质量不再变化
C.百分含量w(NH3)=w(NO)
D.反应速率v(NH3)∶v(O2)∶v(NO)∶v(H2O)=4∶5∶4∶6
E.恒压条件下,混合气体的密度不再变化
(2)2A ![]() B+C在某一温度达到平衡,若A是气态,加压平衡不移动,则B为______态。
B+C在某一温度达到平衡,若A是气态,加压平衡不移动,则B为______态。
(3)已知在一定温度下,C(s)+CO2(g) ![]() 2CO(g)平衡常数K;K的表达式__________;C(s)+H2O(g)CO(g)+H2(g)平衡常数K1;CO(g)+H2O(g)
2CO(g)平衡常数K;K的表达式__________;C(s)+H2O(g)CO(g)+H2(g)平衡常数K1;CO(g)+H2O(g)![]() H2(g)+CO2(g)平衡常数K2;则K、K1、K2之间的关系是:K=_____________;
H2(g)+CO2(g)平衡常数K2;则K、K1、K2之间的关系是:K=_____________;
(4)如图1所示,在甲、乙两容器中都充入1mol C和1mol CO2,并使甲、乙两容器初始容积相等.在相同温度下发生反应C(s)+CO2(g)![]() 2CO(g),并维持反应过程中温度不变.已知甲容器中CO2的转化率随时间变化的图象如图2所示,请在图2中画出乙容器中CO2的转化率随时间变化的图象________.
2CO(g),并维持反应过程中温度不变.已知甲容器中CO2的转化率随时间变化的图象如图2所示,请在图2中画出乙容器中CO2的转化率随时间变化的图象________.


查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国科学家成功研制出新型铝-石墨烯(Cn)可充电电池,电解质为阳离子(EMIM+)与阴离子(AlCl4-)组成的离子液体,该电池放电过程示意图如右。下列说法错误的是

A. 放电时铝为负极,发生氧化反应
B. 放电时正极的反应为:Cn+AlCl4--e-=Cn[AlCl4]
C. 充电时石墨烯与电源的正极相连
D. 充电时的总反应为:3Cn+4Al2Cl7-=Al+4AlCl4-+3Cn[AlCl4]
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二氧化氯是高效、低毒的消毒剂。已知:ClO2是一种黄绿色易溶于水的气体,具有强氧化性,回答下列问题:
(1)ClO2的制备及性质探究(如图所示)。

①仪器a的名称为________,装置B的作用是________。
②装置C用于制备ClO2,同时还生成一种酸式盐,该反应的化学方程式为_________。装置D中滴有几滴淀粉溶液,其作用是________________。
③装置E用于吸收尾气,反应生成NaClO2,则该反应中氧化剂与还原剂的物质的量之比为________,氧化产物是___________。
(2)粗略测定生成ClO2的量
实验步骤如下:
a. 取下装置D,将其中的溶液转入250mL容量瓶,用蒸馏水洗涤D瓶2~3次,并将洗涤液一并转移到容量瓶中,再用蒸馏水稀释至刻度。
b. 从容量瓶中取出25.00mL溶液于锥形瓶中,用0.1000mol/L硫代硫酸钠标准溶液滴定(I2+2S2O32-=2I-+S4O62-),指示剂显示终点时共用去24.00 mL硫代硫酸钠溶液。
①滴定至终点的现象是_____________。
②进入装置D中的ClO2质量为_______,与C中ClO2的理论产量相比,测定值偏低,可能的原因是__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,反应N2O4(g)![]() 2NO2(g)△H>0,在密闭容器中达到平衡。下列说法不正确的是( )
2NO2(g)△H>0,在密闭容器中达到平衡。下列说法不正确的是( )
A. 加压时(体积变小),将使正反应速率增大
B. 保持体积不变,升高温度,再达平衡时颜色变深
C. 保持体积不变,加入少许N2O4,再达到平衡时,颜色变深
D. 保持体积不变,加入少许NO2,将使正反应速率减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高温下,粗硅与纯净的氯气反应,生成四氯化硅(SiCl4),再用氢气还原四氯化硅得到高纯硅。某实验小组在实验室制备并收集四氯化硅,装置示意图如下:

(查阅资料)四氯化硅极易与水反应,其熔点为-70.0℃,沸点为57.7℃。
回答下列问题:
(1)①装置A用于制备氯气,应选用下列哪个装置___________(填序号)。

②装置A中反应的离子方程式为____________________________________。
(2)装置B中X试剂是_________(填名称)。
(3)装置E中冰水混合物的作用是______________________________________。
(4)某同学为了测定四氯化硅的纯度,取所得四氯化硅样品mg,用氢气在高温下还原,得到高纯硅ng,则样品中四氯化硅的纯度是___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,是一个制取氯气并以氯气为原料进行特定反应的装置,其中各试剂瓶装的试剂为:B(AgNO3溶液)、C(氯化亚铁溶液)、D(碘化钾淀粉溶液)、E(水)、H(紫色石蕊试液)
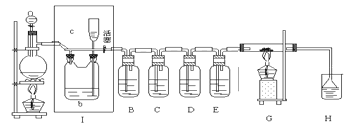
(1)A是氯气发生装置,蒸馏烧瓶中盛放MnO2固体,其化学反应方程式是:________
(2)实验开始时,先点燃A处酒精灯,打开分液漏斗旋塞和Ⅰ处活塞,让氯气充满整个装置,再点燃G处酒精灯,回答下列问题:
下列装置中的现象是B________;D________请写出C中发生反应的化学方程式________
(3)在G装置的硬质玻璃管内盛有碳粉,发生氧化还原反应,一种产物能使H处紫色石蕊试液变红,另一产物能使澄清石灰水变浑浊,写出G中的反应的化学方程式________。
(4)在H处,紫色石蕊试液的颜色由紫色变为红色,再变为无色,其原因是________。
(5)G处反应完毕后关闭分液漏斗旋塞,移去酒精灯,但由于余热的作用,A处仍有氯气产生,此时应该怎样操作________;装置Ⅰ中的现象是________。
(6)若将E中的水换成氢氧化钠溶液,溶液中不但有NaClO还有NaClO3 , 其物质的量比为1:2,则氧化剂和还原剂的物质的量之比为:________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com