
 .
. 分析 0.05mol某烃完全燃烧,将全部产物依次通入足量的浓硫酸和碱石灰,浓硫酸增重5.4g,碱石灰增重11g,
生成水的物质的量为n(H2O)=$\frac{5.4g}{18g/mol}$=0.3mol,n(H)=2n(H2O)=0.3mol×2=0.6mol,
生成CO2的物质的量为n(CO2)=$\frac{11g}{44g/mol}$=0.25mol,所以n(C)=n(CO2)=0.25mol,
则有机物中N(C)=$\frac{0.25mol}{0.05mol}$=5,N(H)=$\frac{0.6mol}{0.05mol}$=12,分子式为C5H12,该烃的一氯代物只有一种,说明只有一种H原子,以此解答该题.
解答 解:(1)0.05mol某烃完全燃烧,将全部产物依次通入足量的浓硫酸和碱石灰,浓硫酸增重5.4g,碱石灰增重11g,
生成水的物质的量为n(H2O)=$\frac{5.4g}{18g/mol}$=0.3mol,n(H)=2n(H2O)=0.3mol×2=0.6mol,
生成CO2的物质的量为n(CO2)=$\frac{11g}{44g/mol}$=0.25mol,所以n(C)=n(CO2)=0.25mol,
则有机物中N(C)=$\frac{0.25mol}{0.05mol}$=5,N(H)=$\frac{0.6mol}{0.05mol}$=12,分子式为C5H12,
故答案为:C5H12;
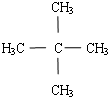
(2)分子中只有一种H原子,C5H12是烷烃,所以H原子一定位于甲基上,所以甲基数目为$\frac{12}{3}$=4,剩余的1个C原子通过单键连接4个甲基,结构简式为 ,
,
故答案为: .
.
点评 本题考查有机物分子式的确定、限制条件同分异构体的书写,为高频考点,侧重于学生的分析、计算能力的考查,题目中等,注意利用等效H确定含有的甲基数目,书写结构式.


科目:高中化学 来源: 题型:选择题
| A. | 煤中含有苯和甲苯,可用先干馏后分馏的方法将它们分离出来 | |
| B. | 含C18以上烷烃的重油经过催化裂化可以得到汽油 | |
| C. | 煤是由有机物和无机物组成的复杂混合物 | |
| D. | 石油含有C5~C11的烷烃,可以通过石油的分馏得汽油 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | Va>Vb时:c (CH3COOH)>c (CH3COO-)>c (K+) | |
| B. | Va=Vb时:c (CH3COOH)+c (H+)>c (OH-) | |
| C. | Va<Vb时:c (CH3COO-)>c (K+)>c (OH-)>c (H+) | |
| D. | Va与Vb任意比时:c (K+)+c (H+)=c (OH-)+c (CH3COO-) |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

| 操作步骤 | 现象 |
| 步骤1:向2mL 0.005mol•L-1 AgNO3溶液中加入2mL 0.005mol•L-1 KSCN溶液,静置 | 出现白色沉淀 |
| 步骤2:取1mL上层清液于试管中,滴加1滴2mol•L-1 Fe(NO3)3溶液 | 溶液变红色 |
| 步骤3:向步骤2的溶液中,继续加入5滴3mol•L-1 AgNO3溶液 | 现象a出现白色沉淀,溶液红色变浅 |
| 步骤4:向步骤1余下的浊液中加入5滴3mol•L-1 KI溶液 | 出现黄色沉淀 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该元素的电负性是同主族最大的 | |
| B. | 其轨道表示式为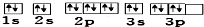 | |
| C. | 该元素的第一电离能是同周期元素中最大的 | |
| D. | 该元素可以形成2种常见的氧化物 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
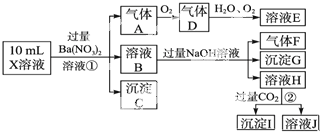
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,5.6 L CO2与足量Na2O2反应转移的电子数为0.5 NA | |
| B. | 78 g苯含有碳碳双键的数目为3 NA | |
| C. | 常温下,4.4gCO2和N2O混合物中所含有的原子数为0.3 NA | |
| D. | 1 L 1 mol•L-1的CuSO4溶液中含NA个Cu2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH4 | B. | C2H4 | C. | C2H6 | D. | C2H6O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 升高温度,正反应速率减小,逆反应速率增大 | |
| B. | 降低温度,正反应速率增大,逆反应速率减小 | |
| C. | 增大压强,正、逆反应速率都增大 | |
| D. | 减小压强,正、逆反应速率都不变 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com