
分析 依据原电池工作原理解答:原电池是将氧化还原反应分成两个半反应,分别在两个电极发生,将化学能转化为电能的装置,原电池负极为电子流出极,发生氧化反应,正极为电子流入极,发生还原反应,外电路电子在导线中定向移动,内电路中电解质中的阴阳离子定向移动,形成闭合回路;
根据电池总反应可知,放电时,Fe被氧化生成Fe(OH)2,电极反应式为Fe-2e-+2OH-=Fe(OH)2,正极NiO2得电子被还原生成Ni(OH)2,电极反应式为NiO2+2H2O+2e-=Ni(OH)2+2OH-,充电时电能转化为化学能,电极反应与原电池电极反应相反,以此解答该题.
解答 解:原电池是将氧化还原反应分成两个半反应,分别在两个电极发生,将化学能转化为电能的装置,原电池负极为电子流出极,发生氧化反应,正极为电子流入极,发生还原反应,外电路电子在导线中定向移动,内电路中电解质中的阴阳离子定向移动,形成闭合回路;
某可逆电池的总反应方程式为:Fe+NiO2+2H2O $\stackrel{KOH}{?}$Fe(OH)2+Ni(OH)2,电解液是氢氧化钾溶液,放电时,Fe是还原剂,被氧化生成Fe(OH)2,电极反应式为Fe-2e-+2OH-=Fe(OH)2,放电时氧化剂是NiO2得电子被还原生成Ni(OH)2,电极反应式为NiO2+2H2O+2e-=Ni(OH)2+2OH-,
故答案为:氧化还原反应;化学;电;负;氧化;正;还原;使溶液导电,形成闭合回路;氢氧化钾溶液;Fe;Fe-2e-+2OH-=Fe(OH)2;NiO2;NiO2+2H2O+2e-=Ni(OH)2+2OH-.
点评 本题考查了原电池工作的原理,题目难度不大,侧重考查学生对基础知识的掌握.


 导学全程练创优训练系列答案
导学全程练创优训练系列答案科目:高中化学 来源: 题型:选择题
| A. | 元素原子半径大小呈周期性变化 | |
| B. | 元素原子量依次递增 | |
| C. | 元素的最高正化合价呈周期性变化 | |
| D. | 元素原子最外层电子排布呈周期性变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 盐酸、空气、醋酸、干冰 | B. | 冰醋酸、碱石灰、硫酸钠、乙醇 | ||
| C. | 蛋白质、油脂、苛性钠、石灰石 | D. | 胆矾、漂白粉、氯化钾、硫酸钡 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
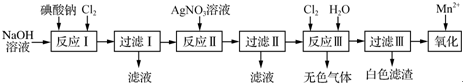
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

查看答案和解析>>
科目:高中化学 来源: 题型:填空题
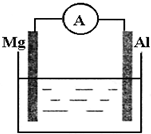 如图所示装置
如图所示装置 查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③ | B. | ②③④ | C. | ①④ | D. | ①②④ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ;B的结构简式为
;B的结构简式为 ;与A含有相同种类和数目的官能团(包括苯环)、且苯环上取代基位置和数量也相同的同分异构体有多种,写出其中任意一种的结构简式
;与A含有相同种类和数目的官能团(包括苯环)、且苯环上取代基位置和数量也相同的同分异构体有多种,写出其中任意一种的结构简式 (不包括原化合物,不考虑立体异构).
(不包括原化合物,不考虑立体异构).查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com