
利用铝灰(主要成分为Al、Al2O3、AlN、FeO等)制备铝鞣剂【主要成分为Al(OH)2Cl】的一种工艺如下:
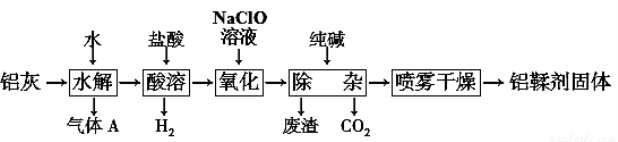
⑴气体A能使湿润的红色石蕊试纸变蓝。铝灰在90 ℃水解生成A的化学方程式为: 。
⑵“酸溶”时,Al2O3发生反应的离子方程式为: 。
⑶“氧化”时,发生反应的离子方程式为: 。
⑷“废渣”成分为________(填化学式)。
⑸采用喷雾干燥而不用蒸发的原因是______________________。
⑹煅烧硫酸铝铵晶体,发生的主要反应为:
4[NH4Al(SO4)2·12H2O]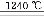 2Al2O3+2NH3↑+N2↑+5SO3↑+3SO2↑+53H2O
2Al2O3+2NH3↑+N2↑+5SO3↑+3SO2↑+53H2O
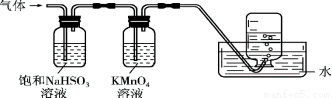
将产生的气体通过如下图所示的装置。则集气瓶中收集到的气体是 (填化学式)。
科目:高中化学 来源:2017届北京市海淀区高三上学期期末化学试卷(解析版) 题型:实验题
为探究FeCl3溶液中的离子平衡和离子反应,某小组同学进行了如下实验。
(1)配制50 mL 1.0 mol·L?1的FeCl3溶液,测其pH约为0.7,即c(H+) = 0.2 mol·L?1。
① 用化学用语解释FeCl3溶液呈酸性的原因: 。
② 下列实验方案中,能使FeCl3溶液pH升高的是 (填字母序号)。
a. 加水稀释 b. 加入FeCl3固体
c. 滴加浓KSCN溶液 d. 加入NaHCO3固体
(2)小组同学利用上述FeCl3溶液探究其与足量锌粉的反应。实验操作及现象如下:
操作 | 现象 |
向反应瓶中加入6.5 g锌粉,然后加入50 mL 1.0 mol·L?1的FeCl3溶液,搅拌 | 溶液温度迅速上升,稍后出现红褐色沉淀,同时出现少量气泡;反应一段时间后静置,上层溶液为浅绿色,反应瓶底部有黑色固体 |
收集检验反应过程中产生的气体 | 集气管口靠近火焰,有爆鸣声 |
已知:Zn的性质与Al相似,能发生反应:Zn + 2NaOH = Na2ZnO2 + H2 ↑
① 结合实验现象和平衡移动原理解释出现红褐色沉淀的原因: 。
② 用离子方程式解释反应后溶液为浅绿色的原因: 。
③ 分离出黑色固体,经下列实验证实了其中含有的主要物质。
i. 黑色固体可以被磁铁吸引;
ii. 向黑色固体中加入足量的NaOH溶液,产生气泡;
iii. 将ii中剩余固体用蒸馏水洗涤后,加入稀盐酸,产生大量气泡;
iv. 向iii反应后的溶液中滴加KSCN溶液,无变化。
a. 黑色固体中一定含有的物质是 。
b. 小组同学认为上述实验无法确定黑色固体中是否含有Fe3O4,理由是 。
(3)为进一步探究上述1.0 mol·L?1 FeCl3溶液中Fe3+和H+氧化性的相对强弱,继续实验并观察到反应开始时现象如下:
操作 | 现象 |
将5 mL 1.0 mol·L?1的FeCl3溶液与0.65 g锌粉混合 | 溶液温度迅速上升,开始时几乎没有气泡 |
将 与0.65 g锌粉混合 | 溶液中立即产生大量气泡 |
小组同学得出结论:在1.0 mol·L?1 FeCl3溶液中,Fe3+的氧化性比H+更强。
查看答案和解析>>
科目:高中化学 来源:2017届广东省肇庆市高三上学期二模化学试卷(解析版) 题型:推断题
[化学—选修3:物质结构与性质]目前半导体生产正在进行一场“铜芯片”革命:在硅芯片上用铜代替铝布线。古老的金属铜在现代科技应用上取得了突破。用黄铜矿(主要成分为CuFeS2)生产粗铜,其反应原理如下:
(1)基态铜原子的价电子排布式为____________,硫、氧元素相比,第一电离能较大的元素是________(填元素符号)。
(2)反应①、②中均生成有相同的气体分子,该分子的中心原子杂化类型是_________,其立体结构是________,与该分子互为等电子体的单质气体的化学式是 。
(3)某学生用硫酸铜溶液与氨水做了一组实验:CuSO4溶液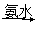 蓝色沉淀
蓝色沉淀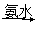 沉淀溶解,得到深蓝色透明溶液。生成蓝色沉淀溶于氨水的离子方程式为 ;
沉淀溶解,得到深蓝色透明溶液。生成蓝色沉淀溶于氨水的离子方程式为 ;
(4)铜是第四周期最重要的过渡元素之一,其单质及化合物具有广泛用途。铜晶体中铜原子堆积模型为________;铜的某种氧化物晶胞结构如图所示,若该晶体的密度为d g/cm3,阿伏加德罗常数的值为NA,则该晶胞中铜原子与氧原子之间的距离为________pm。(用含d和NA的式子表示)

查看答案和解析>>
科目:高中化学 来源:2017届广东省肇庆市高三上学期二模化学试卷(解析版) 题型:选择题
下列根据实验操作和现象得出的结论正确的是( )
选项 | 实验操作 | 实验现象 | 结论 |
A | 将少量Fe(NO3)2试样加水溶解后,滴加稀硫酸酸化,再滴加KSCN溶液 | 溶液变成血红色 | Fe(NO3)2试样已变质 |
B | 向甲苯中滴加少量酸性高锰酸钾溶液 | 高锰酸钾溶液褪色 | 甲苯发生了氧化反应 |
C | 常温下分别测定浓度均为0.1mol/L的Na2SiO3溶液和Na2CO3溶液的pH | pH:Na2SiO3>Na2CO3 | 非金属性:Si>C |
D | 将少量某无色气体通入澄清石灰水中 | 出现白色沉淀 | 该气体一定是CO2 |
查看答案和解析>>
科目:高中化学 来源:2017届广东省深圳市三校高三上学期第一次联考化学卷(解析版) 题型:选择题
分子式为C5H10O2,并能与饱和NaHCO3溶液反应放出气体的有机物有多少种(不含立体异构)( )
A.3 种 B.4 种 C.5 种 D.6 种
查看答案和解析>>
科目:高中化学 来源:2017届广东省深圳市三校高三上学期第一次联考化学卷(解析版) 题型:选择题
下列物质间的转化关系中不能全部通过一步反应完成的是( )
A.Na→NaOH→Na2CO3→NaCl
B.Mg→MgCl2→MgCO3→Mg(OH)2
C.Al→Al2O3→Al(OH)3→AlCl3
D.Fe→FeCl3→Fe(OH)3→Fe2O3
查看答案和解析>>
科目:高中化学 来源:2017届广东省韶关市高三上高考调研理综化学试卷(解析版) 题型:选择题
某有机物分子式为C4H8,据此推测其结构和性质均正确的是
A.它与乙烯一定是同系物
B.它一定能使溴水褪色
C.它的一氯代物可能只有一种
D.等质量CH4和C4H8分别在氧气中完全燃烧,CH4的耗氧量小于C4H8
查看答案和解析>>
科目:高中化学 来源:2017届四川省绵阳市高三1月诊断性考试化学试卷(解析版) 题型:选择题
用FeS2纳米材料制成的高容量锂电池,电极分别是二硫化亚铁和金属锂,电解液是含锂盐的有机溶剂。下列说法错误的是
A.金属锂作电池的负极
B.电池正极反应为FeS2+4Li++4e-==Fe+2Li2S
C.放电时,Li+向负极迁移
D.电池总反应为FeS2+4Li ==Fe+2Li2S
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com