
【题目】回答下列问题:
(1)1 mol CO2中含有的σ键数目为________,π键数目为________。
(2)已知CO和CN-与N2结构相似,CO分子内σ键与π键个数之比为________。CH2=CHCN分子中σ键与π键数目之比为________。
(3)肼(N2H4)分子可视为NH3分子中的—个氢原子被-NH2(氨基)取代形成的另一种氮的氢化物。肼可用作火箭燃料,燃烧时发生的反应:N2O4(l)+2N2H4(l)===3N2(g)+4H2O(g) ΔH=-1 038.7 kJ·mol-1若该反应中有4 mol N—H键断裂,则形成的π键有________mol。
(4)Co 基态原子核外电子排布式为____________;
基态Ge原子的核外电子排布式为____________;
Zn2+的价电子轨道表示式为_______________;
Co3+核外电子未成对电子数为__________________。
(5)CH4、NH3、H2O、HF分子中共价键的极性由强到弱的顺序是_______________________。
【答案】2NA 2NA 1:2 2:1 3 1s22s22p63s23p63d74s2 1s22s22p63s23p63d104s24p2;  4 HF>H2O>NH3>CH4
4 HF>H2O>NH3>CH4
【解析】
(1) CO2的结构式是O=C=O,1个二氧化碳分子中有2个碳氧双键,双键中有1个σ键和1个π键,1 mol CO2中含有的σ键数目为2NA,π键数目为2NA。
(2) N2的结构式是N![]() N,三键中1个σ键和 2个π键,已知CO和CN-与N2结构相似,CO分子内存在C
N,三键中1个σ键和 2个π键,已知CO和CN-与N2结构相似,CO分子内存在C![]() O键,σ键与π键个数之比为1:2。CH2=CHCN分子的结构式是
O键,σ键与π键个数之比为1:2。CH2=CHCN分子的结构式是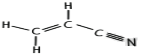 ,分子中有6个σ键和3个π键,σ键与π键数目之比为2:1。
,分子中有6个σ键和3个π键,σ键与π键数目之比为2:1。
(3) N2的结构式是N![]() N,三键中1个σ键和 2个π键,产物中只有N2含有π键;肼(N2H4)分子中含有4个N-H键。燃烧时发生的反应:N2O4(l)+2N2H4(l)===3N2(g)+4H2O(g) ΔH=-1 038.7 kJ·mol-1,若该反应中有4 mol N—H键断裂,则消耗1mol N2H4,生成1.5mol N2,形成的π键有3mol。
N,三键中1个σ键和 2个π键,产物中只有N2含有π键;肼(N2H4)分子中含有4个N-H键。燃烧时发生的反应:N2O4(l)+2N2H4(l)===3N2(g)+4H2O(g) ΔH=-1 038.7 kJ·mol-1,若该反应中有4 mol N—H键断裂,则消耗1mol N2H4,生成1.5mol N2,形成的π键有3mol。
(4)Co 是27号元素,核外有27个电子,根据能量最低原理,其核外电子排布式为1s22s22p63s23p63d74s2;
Ge是32号元素,基态Ge原子的核外电子排布式为1s22s22p63s23p63d104s24p2;
Zn是30号元素,Zn价电子排布式是3d104s2,Zn2+的价电子排布式是3d10,Zn2+价电子轨道表示式为 ;
;
Co3+核外电子排布式是1s22s22p63s23p63d6,Co3+的价电子排布图是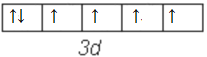 ,Co3+核外电子未成对电子数为4。
,Co3+核外电子未成对电子数为4。
(5)同周期元素从左到右电负性增强,原子吸引电子能力增强,所以CH4、NH3、H2O、HF分子中共价键的极性由强到弱的顺序是HF>H2O>NH3>CH4。


 冲刺100分1号卷系列答案
冲刺100分1号卷系列答案科目:高中化学 来源: 题型:
【题目】下列关于有机化合物M和N的说法正确的是
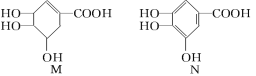
A.等物质的量的两种物质跟足量的NaOH反应,消耗NaOH的量相等
B.完全燃烧等物质的量的两种物质生成二氧化碳和水的量分别相等
C.一定条件下,两种物质都能发生酯化反应和氧化反应
D.N分子中,可能在同一平面上的原子最多有14个
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2009年《化学教育》期刊封面刊载如图所示的有机物M(只含C、H、O)的球棍模型图。不同大小、颜色的小球代表不同的原子,小球之间的“棍”表示共价键,既可以表示三键,也可以表示双键,还可以表示单键。下列有关M的推断正确的是( )
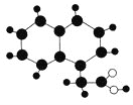
A. M的分子式为C12H12O2
B. M与足量氢气在一定条件下反应的产物的环上一氯代物有7种
C. M能发生中和反应、取代反应
D. 一个M分子最多有11个原子共面
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海冰是海水冻结而成的咸水冰。海水冻结时,部分来不及流走的盐分以卤汁的形式被包围在冰晶之间,形成“盐泡”![]() 假设盐分以一个NaCl计
假设盐分以一个NaCl计![]() ,其大致结构如下图所示,若海冰的冰龄达到1年以上,融化后的水为淡水。下列叙述正确的是( )
,其大致结构如下图所示,若海冰的冰龄达到1年以上,融化后的水为淡水。下列叙述正确的是( )

A.海冰内层“盐泡”越多,密度越小
B.海冰冰龄越长,内层的“盐泡”越多
C.海冰内层“盐泡”内的盐分主要以NaCl分子的形式存在
D.海冰内层NaCl的浓度约为![]() 设冰的密度为
设冰的密度为![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有一种新型燃料电池,工作时在一极通入空气,另一极通入丁烷气体;电解质是掺杂氧化钇(Y2O3)的氧化锆(ZrO2)晶体,在熔融状态下能传导O2-。现用该燃料电池和惰性电极电解Na2SO4溶液一段时间,假设电解时温度不变,下列说法不正确的是( )
A.在熔融电解质中,O2-由正极移向负极
B.通入空气的一极是正极,电极反应式为O2+4e-=2O2-
C.电解池的阳极反应式为2H2O-4e-=4H++O2↑
D.电解一共生成0.9mol气体时,理论上消耗0.1mol丁烷
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有七种元素,其中A、B、C、D、E为短周期主族元素,F、G为第4周期元素,它们的原子序数依次增大。请根据下列相关信息,回答问题。
元素 | 相关信息 |
A | 元素的核外电子数和电子层数相等,也是宇宙中最丰富的元素 |
B | 元素原子的核外p电子数比s电子数少1 |
C | 原子的第一至第四电离能分别是I1=738 kJ·mol-1; I2=1 451 kJ·mol-1;I3=7 733 kJ·mol-1;I4=10 540 kJ·mol-1 |
D | 原子核外所有p轨道全满或半满 |
E | 元素的主族序数与周期数的差为4 |
F | 是前四周期中电负性最小的元素 |
G | 在周期表的第七列 |
(1)B基态原子中能量最高的电子,其电子云在空间有______个伸展方向,原子轨道呈________形。
(2)某同学根据上述信息,推断C基态原子的轨道表示式为![]() 该同学所画的轨道表示式违背了________________。
该同学所画的轨道表示式违背了________________。
(3)G位于______族__________区,价电子排布式为________________。
(4)检验F元素的方法是________,请用原子结构的知识解释产生此现象的原因:_____________。
(5)写出E的单质与水反应的离子方程式:_____________________________________
(6)写出DA3的电子式_______________________(用元素符号)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】维生素C(VitaminC)又名抗坏血酸,具有酸性和强还原性,也是一种常见的食品添加剂,其结构如图。下列有关说法中正确的是
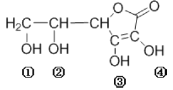
A.维生素C的分子式为C5H8O6
B.维生素C的酸性可能是③、④两个羟基引起的
C.维生素C中含有醚键
D.维生素C与足量的金属钠反应产生氢气的物质的量是维生素C的4倍
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】汽车尾气中含有CO、NO、NO2、碳氢化合物等多种污染物。回答下列问题:
(1)汽车燃料中不含氮元素,尾气中所含NO产生的原因是_________________________(用化学方程式表示)。
(2)已知:2C4H10(g)+13O2(g)=8CO2(g)+10H2O(g) △H1=-5316 kJ·mol-1
N2(g)+O2(g)=2NO(g) △H2
2NO(g)+2CO(g)=N2(g)+2CO2(g) △H3=-746 kJ·mol-1
①若H2O(l)=H2O(g) △H=+44 kJ·mol-1,则表示正丁烷燃烧热的热化学方程式为__________________。
②部分化学键键能数据为:氧分子中氧氧键的键能为494 kJ·mol-1;C=O的键能为799 kJ·mol-1;CO分子中碳氧键的键能为1076 kJ·mol-1;请计算出反应2CO(g)+O2(g)=2CO2(g)的△H=______________kJ·mol-1,由此可以计算△H2=__________kJ·mol-1
(3)1573K时,N2+O2![]() 2NO平衡常数为2.0×10-6,若测得内燃机内平衡混合气中氮气、氧气的物质的量分别为0.2mol、0.001mol,则生成NO的物质的量为_____________mol,N2的转化率为____________。
2NO平衡常数为2.0×10-6,若测得内燃机内平衡混合气中氮气、氧气的物质的量分别为0.2mol、0.001mol,则生成NO的物质的量为_____________mol,N2的转化率为____________。
(4)T<500K时,反应NO2(g)+CO(g)=NO(g)+CO2(g)分两步进行:
第一步:NO2(g)+NO2(g)=NO3(g)+NO(g) (慢反应)
第二步:NO3(g)+CO(g)=NO(g)+CO2(g) (快反应)
下列表述正确的是__________(填标号)
A.反应速率与NO2浓度有关 B.反应速率与NO浓度有关
C.反应的中间产物只有NO3 D.第一步反应活化能较低
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】纳米磷化钴(CoP)常用于制作特种钻玻璃,制备磷化钴的常用流程如下:
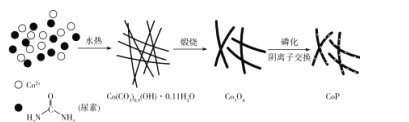
(l)基态P原子的价电子排布式为____,P位于元素周期表中____区。
(2)尿素中N原子的杂化类型是 _____;C、N、O三种元素的第一电离能最大的是____,电负性由小到大的顺序为____。
(3)Co(CO3)0.5(OH)·0.11H2O中CO32-中C的价层电子对数为____;该化合物中不含有的化学键有_____填标号)。
A 离子键 B 共价键 C 金属键 D 配位键 E 氢键 F 非极性键
(4)一些氧化物的熔点如下表所示:
![]()
解释表中氧化物之间熔点差异的原因____。
(5)CoP的晶胞结构如图所示,最近且相邻两个钴原子的距离为npm。
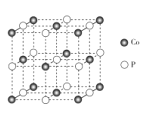
设NA为阿伏加德罗常数的值,则其晶胞密度为_______-g.cm-3(列出计算式即可)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com