
| A. | CO32-+H+=HCO3- | B. | HCO3-+3CO32-+7H+═4CO2↑+4H2O | ||
| C. | 2HCO3-+5CO32-+12H+═7CO2↑+7H2O | D. | HCO3-+CO32-+3H+═2CO2↑+2H2O |
分析 碳酸氢根离子、碳酸根离子加入盐酸,碳酸根离子先与氢离子反应生成碳酸氢根离子,然后碳酸氢根离子再反应生成二氧化碳和水,据此解答.
解答 解:A.当滴入少量稀盐酸时,碳酸根离子优先反应,发生反应的离子方程式为:CO32-+H+→HCO3-,故A正确;
B.设原物质中含有3mol碳酸根离子,则含有1.5mol碳酸氢根离子,加入7mol氢离子,先与3mol碳酸根离子反应生成3mol碳酸氢根离子,剩余盐酸不足,与部分4mol碳酸氢根离子反应生成二氧化碳,离子方程式:HCO3-+3CO32-+7H+═4CO2↑+4H2O,故B正确;
C.设原物质中含有碳酸根离子5mol,则含有2.5mol碳酸氢根离子,加入12mol氢离子,先与5mol碳酸根离子反应生成5mol碳酸氢根离子,剩余7mol氢离子再与7mol碳酸氢根离子反应生成7mol二氧化碳,离子方程式:2HCO3-+5CO32-+12H+═7CO2↑+7H2O,故C正确;
D.设原固体中含有碳酸根离子,1mol则含有碳酸氢根离子0.5mol,加入3mol氢离子,先与1mol碳酸根离子反应生成1mol碳酸氢根离子,剩余2mol氢离子与1.5mol碳酸氢根离子反应生成1.5mol二氧化碳,氢离子剩余,离子方程式:0.5HCO3-+CO32-+2.5H+═1.5CO2↑+1.5H2O,化简为:HCO3-+2CO32-+5H+═2CO2↑+3H2O,故D错误;
故选:D.
点评 本题考查了离子方程式的书写,题目难度中等,注意掌握离子方程式的书写原则,明确碳酸根离子、碳酸氢根离子与氢离子反应的先后顺序为解答关键,本题中还需要明确碳酸氢根离子、碳酸根离子的物质的量之比为1:2.


 走进文言文系列答案
走进文言文系列答案科目:高中化学 来源: 题型:选择题
| A. | 质量为32g | B. | 含氧原子数为NA | ||
| C. | 含氧分子数为NA | D. | 在标准状况下,体积约为22.4L |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 标准状况下,22.4 L H2含有的原子数是2NA | |
| B. | 标准状况下,NA个水分子的体积是22.4 L | |
| C. | 任何情况下,1 mol CO中都含有NA个分子 | |
| D. | 通常状况下,NA个NH3分子的体积是22.4 L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分别配成1mol/L的溶液,各取1mL滴加1滴酚酞试液,比较颜色深浅 | |
| B. | 分别取样在试管中加热,将可能产生的气体通入澄清石灰水,观察有无白色浑浊 | |
| C. | 分别取样配成溶液,滴加Ba(OH)2溶液,观察有无白色沉淀 | |
| D. | 分别配成溶液,用铂丝蘸取溶液在酒精灯火焰上灼烧,观察火焰的颜色(必要时可透过蓝色钴玻璃) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
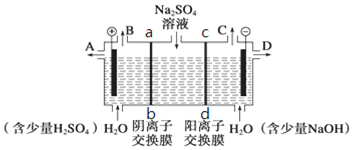
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
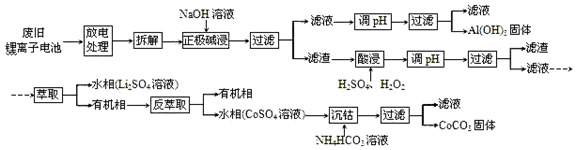
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙炔通入溴水中 | |
| B. | 乙烯通入酸性高锰酸钾溶液中 | |
| C. | 在镍作催化剂的条件下,苯与氢气反应 | |
| D. | 乙烷与氯气光照下发生反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
 A、B、C是单质,其中A是金属,各种物质间的转化关系如图:
A、B、C是单质,其中A是金属,各种物质间的转化关系如图:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com