
 ����أ�KC1O3����������أ�KClO2�������ת����KClO2�ڼ��Ի��������ȶ����ڣ�����KClO2����Ҫ������ͼ��ʾ��
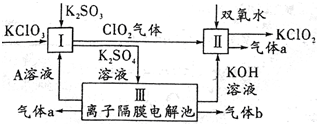
����أ�KC1O3����������أ�KClO2�������ת����KClO2�ڼ��Ի��������ȶ����ڣ�����KClO2����Ҫ������ͼ��ʾ������ ������ͼ��֪���������Ӹ�Ĥ���أ�����������Һ�����ǵ��ˮ������a����ҺA��ͬһ�缫�õ���KOH������b������缫�õ�����AΪ���ᣬaΪ������bΪ������I��KClO3��K2SO3�����ᷴӦ����C1O2��K2SO4��Һ����Ӧ���ӷ���ʽΪ��2H++SO32-+2ClO3-=2C1O2+SO42-+H2O������C1O2����������ڼ��������·�Ӧ����KClO2��������
��1��KC1O2������������Ư�ף������������ǿ�����ԣ�
��2��������������֪�����з�����Ӧ��2ClO2+H2O2+2OH-=2ClO2-+O2��+2H2O����������ȫ����ԭ�����ã����OԪ�ػ��ϼ۱仯����ת�Ƶ��ӣ�
��3������������Һ�����ǵ��ˮ�������������������������Ӹ�Ĥ��������������һ�ˣ�ͬʱ�õ����
��4��C1O2������KClO3�������ǿ���������Ʊ���ClԪ�ػ��ϼ۽��ͣ���CԪ�ر�����Ϊ������̼�����м������ɣ���������ο���Ϊũҵ�ϵļطʣ���ũҵ�Ͽ���ͨ���ڴ���������CO2�ĺ��������ֲ��Ĺ�����ã�
��5��KC1O2��Fe2+����ΪFe3+��KC1O2������ΪCl-������31.95g KC1O2�����ʵ��������ݵ���ת���غ��������Fe2+�����ʵ�����
���ʷ�����Ӧ��3KClO2=2KClO3+KCl��3molKClO2���ʵõ�2mol KClO3��������FeSO4��Һ��Ӧʱ��KClO2��KClO3����Fe2+��ԭΪCl-������3molKClO2��2mol KClO3��Ӧ��õ�����Ŀ��
��� �⣺������ͼ��֪���������Ӹ�Ĥ���أ�����������Һ�����ǵ��ˮ������a����ҺA��ͬһ�缫�õ���KOH������b������缫�õ�����AΪ���ᣬaΪ������bΪ������I��KClO3��K2SO3�����ᷴӦ����C1O2��K2SO4��Һ����Ӧ���ӷ���ʽΪ��2H++SO32-+2ClO3-=2C1O2+SO42-+H2O������C1O2����������ڼ��������·�Ӧ����KClO2��������
��1��KC1O2������������Ư�ף������������ǿ�����ԣ�
�ʴ�Ϊ��ǿ������
��2�����з�Ӧ��������aΪO2�����з�����Ӧ��2ClO2+H2O2+2OH-=2ClO2-+O2��+2H2O��1mol˫��ˮ��Ӧ����1mol��������������ȫ����ԭ�����ã�ת�Ƶ���Ϊ2mol��
�ʴ�Ϊ��O2��2mol��
��3��������������֪��A�Ļ�ѧʽ��H2SO4������������Һ�����ǵ��ˮ��������������������ܷ�ӦʽΪ��2H2O $\frac{\underline{\;���\;}}{\;}$ 2H2��+O2�������������Ӹ�Ĥ��������������һ�ˣ�ͬʱ�õ����ᣬ��������pH���ͣ�
�ʴ�Ϊ��H2SO4��2H2O $\frac{\underline{\;���\;}}{\;}$ 2H2��+O2����������
��4��C1O2������KClO3�������ǿ���������Ʊ���ClԪ�ػ��ϼ۽��ͣ���CԪ�ر�����Ϊ������̼����Ӧ���ӷ���ʽΪ��2ClO3-+H2C2O4+2H+=2ClO2��+2CO2��+2H2O�����м������ɣ���������ο���Ϊũҵ�ϵļطʣ���ũҵ�Ͽ���ͨ���ڴ���������CO2�ĺ��������ֲ��Ĺ�����ã�
�ʴ�Ϊ��2ClO3-+H2C2O4+2H+=2ClO2��+2CO2��+2H2O����������ο���Ϊũҵ�ϵļطʣ���ũҵ�Ͽ���ͨ���ڴ���������CO2�ĺ��������ֲ��Ĺ�����ã�
��5��KC1O2��Fe2+����ΪFe3+��KC1O2������ΪCl-��31.95g KC1O2�����ʵ���Ϊ$\frac{31.95g}{106.5g/mol}$=0.3mol�����ݵ���ת���غ㣬����Fe2+�����ʵ���Ϊ$\frac{0.3mol��4}{1}$=1.2mol��
���ʷ�����Ӧ��3KClO2=2KClO3+KCl��3molKClO2���ʵõ�2mol KClO3��������FeSO4��Һ��Ӧʱ��KClO2��KClO3����Fe2+��ԭΪCl-��3molKClO2��Ӧ��õ���Ϊ3mol��4=12mol��2mol KClO3��Ӧ��õ���Ϊ2mol��6=12mol��������Fe2+���ʵ�����ͬ��
�ʴ�Ϊ��1.2mol����ͬ��
���� ���⿼�������Ʊ�ʵ�飬�ؼ��ǶԹ������̵����⣬�ϺõĿ���ѧ����������������������ȡ��Ϣ������֪ʶǨ��������������5����ע��������ԭ��Ӧ�����е���ת���غ��Ӧ�ã��Ѷ��еȣ�


 ������ҵ����ν�����������ϵ�д�
������ҵ����ν�����������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��Ȼ����û���κ�һ��ʳ����ͬʱ��������Ը���ά���ص���Ҫ | |
| B�� | ����2008�걱�����ˡ����ơ����ı�����һ�����ȼ�� | |
| C�� | �ô�����ľ���һ���������ܷⱣ�棬ʱ��Խ��Խ�㴼 | |
| D�� | �����ǡ����ǡ���ά�غ�֬����һ�������¶����Է���ˮ�ⷴӦ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 64 g•mol-1 | B�� | 24 g•mol-1 | C�� | 56 g•mol-1 | D�� | 188 g•mol-1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | CO 2���ӱ���ģ�ͣ� | B�� | S 2-�Ľṹʾ��ͼ�� | ||
| C�� | ������Ϊ20����ԭ�ӣ�${\;}_{17}^{20}$Cl | D�� | HCN���ӵĽṹʽ��H-C��N |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����

| A�� | 550��ʱ��������������壬v����v�� ����С��ƽ�ⲻ�ƶ� | |
| B�� | 650��ʱ����Ӧ��ƽ���CO2��ת����Ϊ75.0% | |
| C�� | T��ʱ��������������CO2��CO��ƽ��������Ӧ�����ƶ� | |
| D�� | 925��ʱ����ƽ���ѹ����ƽ��Ũ�ȱ�ʾ�Ļ�ѧƽ�ⳣ��Kp=23.04 p�� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com