
分别用一种试剂除去下列各物质中的杂质(括号内为杂质),并写出离子方程式。
(1)BaCl2溶液(HCl)
试剂:________;离子方程式:__________________________ ______________________________________________。
(2)CO2(HCl)
试剂:________;离子方程式:__________________________ ______________________________________________。
 培优好卷单元加期末卷系列答案
培优好卷单元加期末卷系列答案科目:高中化学 来源: 题型:
在无色透明溶液中,下列各离子组能大量共存的是( )
A.SO42- Na+ Fe3+ Cl- B.Ba2+ Na+ Cl- SO42-
C.HCO3- K+ SO42- OH- D.Ag+ Al3+ NO3- H+
查看答案和解析>>
科目:高中化学 来源: 题型:
物质的量浓度相同的NaNO3、Mg(NO3)2、Al(NO3)3三种溶液,取三种溶液的体积比为3:2:1时,三种溶液中c(NO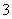 ) 之比为( )
) 之比为( )
A.1:1:1 B.1:2:3
C.3:2:1 D.3:4:3
查看答案和解析>>
科目:高中化学 来源: 题型:
在下列反应中,氧化剂和还原剂为同一种物质的是( )
A.2Na+2H2O===2NaOH+H2↑
B.MnO2+4HCl(浓)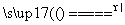 MnCl2+2H2O+Cl2↑
MnCl2+2H2O+Cl2↑
C.Na2CO3+CO2+H2O===2NaHCO3
D.2Na2O2+2CO2===2Na2CO3+O2
查看答案和解析>>
科目:高中化学 来源: 题型:
单质X和Y相互反应生成X2+和Y2-,现有下列叙述:
(a)X被氧化 (b)X是氧化剂
(c)X具有氧化性 (d)Y2-是还原产物
(e)Y2-具有还原性 (f) X2+具有氧化性
其中正确的是( )
A.(a)(b)(c)(d) B.(b)(c)(d)
C.(a)(d)(e)(f) D.(a)(c)(d)(e)
查看答案和解析>>
科目:高中化学 来源: 题型:
实验室也可用KMnO4固体和浓盐酸反应制氯气,反应方程式如下:2KMnO4+16HCl(浓)===2KCl+2MnCl2+8H2O+5Cl2↑。回答下列问题:
(1)该反应中氧化剂是__________,还原产物是____________。
(2)若参加反应的高锰酸钾为7.9 g,被氧化的HCl的物质的量是多少?把生成的氯气全部通入足量氢氧化钠溶液中,生成次氯酸钠多少克?
查看答案和解析>>
科目:高中化学 来源: 题型:
用NA表示阿伏加德罗常数的数值,下列说法正确的是
A.标准状况下,22.4L H2O含有NA个分子
B.1L 1mol·L -1的NaClO 溶液中含有ClO-的数目少于NA个
C.0.1molAlCl3完全转化为氢氧化铝胶体,生成0.l NA个胶体粒子
D.0.1molCl2与足量NaOH溶液反应,转移电子数为0.2 NA
查看答案和解析>>
科目:高中化学 来源: 题型:
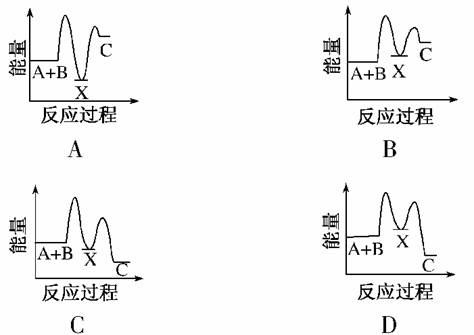
反应A+B—→C(ΔH<0)分两步进行:
①A+B—→X(ΔH>0),②X—→C(ΔH<0)。
下列示意图中,能正确表示总反应过程中能量变化的是( )
查看答案和解析>>
科目:高中化学 来源: 题型:
用CH4催化还原NOx可以消除氮氧化物的污染。已知CH4(g)+4NO2(g)===4NO(g)+CO2(g)+2H2O(g) ΔH=-574 kJ·mol-1,CH4(g)+4NO(g)===2N2(g)+CO2(g)+2H2O(g) ΔH=-1 160 kJ·mol-1。若在标准状况下4.48 L CH4恰好能将一定量NO2还原成N2和H2O(g),则整个过程中放出的热量为( )
A.114.8 kJ B.232 kJ
C.368.8 kJ D.173.4 kJ
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com