
【题目】将2.80 g含氧化镁的镁条完全溶于50.0 mL硫酸溶液后,滴加2.00 mol·Lˉ1氢氧化钠溶液,恰好完全沉淀时用去200.0 mL。将所得的沉淀灼烧、冷却后称量得固体质量为4.40 g。
(1)求上述硫酸的物质的量浓度c(H2SO4)=____________________________。
(2)镁条中氧化镁和镁的物质的量之比为n(MgO)︰n(Mg)=______________。
【答案】4.00 mol·L-1 1:10
【解析】
将含氧化镁的镁条完全溶于硫酸溶液后,发生反应MgO+H2SO4=MgSO4+H2O,Mg+H2SO4=MgSO4+H2↑,滴加2.00mo1/L氢氧化钠液,恰好完全沉淀时用去200.0mL,发生反应MgSO4+2NaOH=Mg(OH)2↓+Na2SO4,将所得的沉淀灼烧、冷却后称量得固体质量为4.40 g,发生反应Mg(OH)2![]() MgO+ H2O,结合反应方程式和原子守恒分析解答。
MgO+ H2O,结合反应方程式和原子守恒分析解答。
(1)将2.80g含氧化镁的镁条完全溶于50.0mL硫酸溶液后,滴加2.00mo1/L氢氧化钠液,恰好完全沉淀时用去200.0mL.可知完全沉淀后,溶液为Na2SO4溶液,根据原子守恒可知,n(SO42-)= ![]() (Na+)=2.0mol/L×0.2L×
(Na+)=2.0mol/L×0.2L×![]() =0.2mol,则硫酸溶液的物质量浓度为
=0.2mol,则硫酸溶液的物质量浓度为![]() =4.00 mol/L,故答案为:4.00 mol/L;
=4.00 mol/L,故答案为:4.00 mol/L;
(2)将所得沉淀灼烧、冷却后称量得固体质量为4.40g,所得固体为MgO,其物质的量为![]() =0.11mol,设Mg的物质的量为x,MgO为y,则x+y=0.11mol,24g/mol×x+40 g/mol×y=4.4g,解得:x=0.1mol,y=0.01mol,则镁条中氧化镁和镁的物质的量之比为n(MgO)∶n(Mg)=0.01mol∶0.1mol=1∶10,故答案为:1∶10。
=0.11mol,设Mg的物质的量为x,MgO为y,则x+y=0.11mol,24g/mol×x+40 g/mol×y=4.4g,解得:x=0.1mol,y=0.01mol,则镁条中氧化镁和镁的物质的量之比为n(MgO)∶n(Mg)=0.01mol∶0.1mol=1∶10,故答案为:1∶10。


科目:高中化学 来源: 题型:
【题目】在恒温恒容容器中:2NO2 ![]() 2NO+O2。不能说明反应达平衡状态的是:
2NO+O2。不能说明反应达平衡状态的是:
①单位时间内生成n mol O2的同时生成2n mol NO2; ②单位时间内生成n mol O2 的同时,生成2n mol NO; ③NO2、NO、O2 的反应速率的比为2 : 2 : 1的状态; ④混合气体的颜色不再改变的状态; ⑤混合气体的密度不再改变的状态; ⑥混合气体的平均相对分子质量不再改变的状态。
A. ①④⑥B. ②③⑤C. ①③④D. ①②③④⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是某学校实验室从化学试剂商店买回的硫酸试剂标签上的部分内容.据此,下列说法正确的是

A. 该硫酸的物质的量浓度为 9.2 mol/L
B. 1 mol Zn与足量的该硫酸反应产生2 g氢气
C. 配制200 mL 4.6 mol/L的稀硫酸需取该硫酸50 mL
D. 该硫酸与等质量的水混合所得溶液的物质的量浓度大于9.2 mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】镭是周期表中第7周期第ⅡA主族元素,下列关于镭的性质描述中不正确的是
A. 在化合物中呈+2价 B. 镭比钙的金属性强
C. 氢氧化物呈两性 D. 碳酸盐难溶于水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】分析化学中常用X射线研究晶体结构,有一种蓝色晶体可表示为:MxFey(CN)z,研究表明它的结构特性是Fe2+、Fe3+分别占据立方体的顶点,自身互不相邻,而CN一位于立方体的棱上,其晶体中的阴离子结构如图示,下列说法正确的是( )
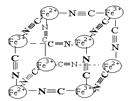
A. 该晶体是原子晶体
B. M的离子位于上述立方体的面心,呈+2价
C. M的离子位于上述立方体的体心,呈+1价,且M+空缺率(体心中没有M+的占总体心的百分比)为50%
D. 晶体的化学式可表示为MFe2(CN)3,且M为+1价
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】决定物质性质的重要因素是物质结构。请回答下列问题。
(1)氯吡苯脲是一种西瓜膨大剂(植物生长调节剂),其组成结构和物理性质见下表。
分子式 | 结构简式 | 外观 | 熔点 | 溶解性 |
C12H10ClN3O |
| 白色结晶粉末 | 170~172 ℃ | 易溶于水 |
查文献可知,可用2-氯-4-氨吡啶与异氰酸苯酯反应,生成氯吡苯脲。
![]()
反应过程中,每生成1 mol氯吡苯脲,断裂____个σ键、断裂____个π键。
(2)过渡金属离子与水分子形成的配合物是否有颜色与其d轨道电子排布有关。一般地,d0或d10排布无颜色,d1~d9排布有颜色。如Co(H2O)6]2+显粉红色。据此判断:Mn(H2O)6]2+_____(填“无”或“有”)颜色。
(3)硼元素具有缺电子性,其化合物往往具有加合性,因而硼酸(H3BO3)在水溶液中能与水反应生成B(OH)4]-而体现一元弱酸的性质,则B(OH)4]-中B的原子杂化类型为_________;
(4)Mg是第三周期元素,该周期部分元素氟化物的熔点见下表:
氟化物 | NaF | MgF2 | SiF4 |
熔点/K | 1 266 | 1 534 | 183 |
解释表中氟化物熔点差异的原因:___________________________________。
(5)我国科学家成功合成了世界上首个五氮阴离子盐(N5)6(H3O)3(NH4)4Cl(用R 代表)。经X-射线衍射测得化合物R 的晶体结构,其局部结构如下图所示。

①组成化合物R 的两种阳离子中σ键的个数之比为____________;其中四核阳离子的立体构型为____________,其中心原子的杂化轨道类型是____________。
②分子中的大π键可用符号表示πmn,其中m 代表参与形成的大π键原子数,n 代表参与形成的大π键电子数,如苯分了中的大π键可表示为π66。则N5-中的大π键应表示为____________。
③请表示出上图中的氢键:________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某离子反应涉及H2O、Cr2O72-、NO2-、H+、NO3-、Cr3+六种微粒,已知反应过程中NO3-浓度变化如图所示,且氧化剂和还原剂的物质的量之比为1∶3,下列判断错误的是( )
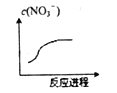
A. Cr2O72-中Cr化合价是+6 价 B. 反应的氧化产物是NO3-
C. 消耗1mol氧化剂,转移电子6mol D. 反应中Cr3+被氧化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验操作、理象和结论均正确的是( )
选项 | 操作 | 现象 | 结论 |
A | 向某溶液中加入NaOH 溶液,并用湿润的红色石蕊试纸检验 | 试纸没有变蓝 | 原溶液中没有有NH4+ |
B | 向苏打和小苏打溶液中分别加入盐酸 | 均冒气泡 | 两者均能与盐酸反应 |
C | 向某溶液中滴加氯水后,再加KSCN溶液 | 溶液变红 | 原溶液中一定有Fe2+ |
D | 向某无色溶液中滴加BaCl2溶液 | 产生白色沉淀 | 该无色溶液中一定含有SO42- |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】胡椒酚是植物挥发油中的一种成分。关于胡椒酚的下列说法:

①该化合物属于芳香烃;
②分子中至少有7个碳原子处于同一平面;
③它的部分同分异构体能发生银镜反应;
④1 mol该化合物最多可与2 mol Br2发生反应。
其中正确的是( )
A. ②③ B. ①②④ C. ①③ D. ②③④
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com