
在容积为2L的容器内,发生反应2A(s)+3B(g)  2C(g)+D(g),起始时充入3molA和2.5molB混合气体;经过5min生成0.5molD,下列说法正确的是
2C(g)+D(g),起始时充入3molA和2.5molB混合气体;经过5min生成0.5molD,下列说法正确的是
A.若单位时间内生成的B和D的物质的量之比为3:1,则体系处于平衡状态
B.C的平衡浓度为2mol/L
C.5min内B的平均消耗速率为0.3mol/(L·min)
D.平衡后,增大压强,平衡向正反应方向移动
 备战中考寒假系列答案
备战中考寒假系列答案科目:高中化学 来源:2017届山东省高三上第一次月考化学试卷(解析版) 题型:选择题
下列实验设计及其对应的离子方程式均正确的是
A.用浓盐酸与铁屑反应制取H2:2Fe+6H+=2Fe3++3H2↑
B.用浓盐酸酸化的KMnO4溶液与H2O2反应,证明H2O2具有还原性:
2MnO4-+6H++5H2O2=2Mn2++5O2↑+8H2O
C.用醋酸除去水垢:CaCO3+2CH3COOH=Ca2++2CH3COO-+H2O+CO2↑;
D.将氯气溶于水制备次氯酸:Cl2+H2O=2H++Cl-+ClO-
查看答案和解析>>
科目:高中化学 来源:2016-2017学年黑龙江佳木斯一中高一上第一次月考化学卷(解析版) 题型:选择题
实验室中需要配制0.1mol/L的CuSO4溶液960ml,以下操作正确的是
A.称取15.36 g CuSO4,加入1000 mL水
B.称取24.0 g CuSO4·5H2O,配成1000 mL溶液
C.称取16.0 g CuSO4,加入1000 mL水
D.称取25 g CuSO4·5H2O,配成1000 mL溶液
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省高二上10月检测化学卷(解析版) 题型:填空题
在容积为10L的密闭容器中,进行如下反应:A(g)+2B(g)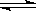 C(g)+D(g),最初加入1.0mol A和2.2mol B,在不同温度下,D的物质的量n(D)和时间t的关系如图1.
C(g)+D(g),最初加入1.0mol A和2.2mol B,在不同温度下,D的物质的量n(D)和时间t的关系如图1.

试回答下列问题:
(1)800℃时,0~5min内,以B表示的平均反应速率为 .
(2)能判断反应达到化学平衡状态的依据是 (填字母).
A.容器中压强不变 B.混合气体中c(A)不变
C.2v正(B)=v逆(D) D.c(A)=c(C)
(3)若最初加入1.0mol A和2.2mol B,利用图中数据计算800℃时的平衡常数K=__________,该反应为__________反应(填“吸热”或“放热”).
(4)700℃时,某时刻测得体系中物质的量浓度如下:n(A)=1.1mol,n(B)=2.6mol,n(C)=0.9mol,n(D)=0.9mol,则此时该反应__________(填“向正方向进行”、“向逆方向进行”或“处于平衡状态”).
(5)在催化剂作用下,CO可用于合成甲醇:CO(g)+2H2(g)?CH3OH(g)若在恒温恒压的条件下,向密闭容器中充入4mol CO和8mol H2,合成甲醇,平衡时CO的转化率与温度、压强的关系如图所示:

①该反应的正反应属于__________反应;(填“吸热”或“放热”).
②在0.1Mpa、100℃的条件下,该反应达到平衡时容器内气体的物质的量为 mol。
若在恒温恒容的条件下,向上述平衡体系中充入4mol CO,8mol H2,与原平衡状态相比,达到平衡时CO转化率 (填“增大”,“不变”或“减小”),平衡常数K (填“增大”,“不变”或“减小”).
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省高二上10月检测化学卷(解析版) 题型:选择题
下列电离方程式正确的是
A.在熔化时NaHSO4 = Na+ + H+ +SO42-
B.H2SO3 2H++SO32-
2H++SO32-
C.NaHCO3 Na++H++CO32-
Na++H++CO32-
D.CaCO3=Ca2++ CO32-
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省高二上10月检测化学卷(解析版) 题型:选择题
在甲酸的下列性质中,可以证明它是弱电解质的是
A.1 mol?L-1甲酸溶液的c(H+)约为1×10-2 mol?L-1
B.甲酸能与活泼金属反应生成氢气
C.10 mL 1 mol?L-1甲酸恰好与10 mL 1 mol?L-1 NaOH溶液完全反应
D.在相同条件下,甲酸溶液的导电性比二元强酸溶液的弱
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省高二上10月检测化学卷(解析版) 题型:选择题
三室式电渗析法处理含Na2SO4废水的原理如图所示,采用惰性电极,ab、cd均为离子交换膜,在直流电场的作用下,两膜中间的Na+和SO42-可通过离子交换膜,而两端隔室中离子被阻挡不能进入中间隔室。

下列叙述正确的是
A.通电后中间隔室的SO42-离子向正极迁移,正极区溶液pH增大
B.该法在处理含Na2SO4废水时可以得到NaOH和H2SO4产品
C.负极反应为2 H2O–4e–=O2+4H+,负极区溶液pH降低
D.当电路中通过1mol电子的电量时,会有0.5mol的O2生成
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山东省高一上10月月考化学卷(解析版) 题型:选择题
设NA为阿伏伽德罗常数的值,下列有关说法不正确的是
A.常温下,48gO3和48gO2含有的原子数目为3NA
B.1molOH-l离子中含电子数目为10 NA
C.0.5L0.2mol·L-1的NaCl溶液中含有的Na+数是0.1 NA
D.33.6LCO中含有的原子总数是3NA
查看答案和解析>>
科目:高中化学 来源:2016-2017学年贵州遵义航天中学高一上月考一化学卷 (解析版) 题型:选择题
某溶液中含有较大量的Cl-、SO42-、OH-等3种阴离子,如果只取一次该溶液就能够分别将3种阴离子依次检验出来,下列实验操作顺序正确的是 ( )
①滴加Mg(NO3)2溶液;②过滤;③滴加AgNO3溶液;④滴加Ba(NO3)2溶液
A.③②④②① B.④②①②③ C.①②③②④ D.④②③②①
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com