
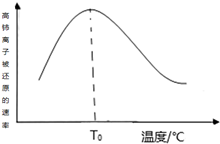
 高铈离子被还原的速率与温度的关系如图所示.图象中,温度高于T0时,高铈离子被还原的速率逐渐减小的原因是高铈离子被还原的反应,正反应为放热反应,开始反应时,反应物浓度大,反应速率快,正反应为放热反应,温度逐渐升高,反应速率加快,温度高于T0℃时,反应物的浓度减少,反应速率减小,温度对反应速率的影响不及浓度的影响.
高铈离子被还原的速率与温度的关系如图所示.图象中,温度高于T0时,高铈离子被还原的速率逐渐减小的原因是高铈离子被还原的反应,正反应为放热反应,开始反应时,反应物浓度大,反应速率快,正反应为放热反应,温度逐渐升高,反应速率加快,温度高于T0℃时,反应物的浓度减少,反应速率减小,温度对反应速率的影响不及浓度的影响. 分析 影响化学反应速率的外界因素:浓度、温度、催化剂等,能使化学反应速率加快的有:升高温度、使用催化剂、有气体参加的反应增大压强、增大反应物浓度、增大反应物的接触面积等.由图可知:温度T0℃为分界点,低于该温度,温度越高,反应速率越大,温度高于T0℃时,温度越高,反应速率越小,由此可知影响该化学反应速率的外界因素为浓度,据此分析解答.
解答 解:影响反应速率的外界因素有浓度、温度、催化剂等,反应物浓度越大,反应速率越大,温度越高,反应速率越大,由图可知:温度T0℃为分界点,低于该温度,温度越高,反应速率越大,温度高于T0℃时,温度越高,反应速率越小,说明高铈离子被还原的反应,正反应为放热反应,开始反应时,温度逐渐升高,反应速率加快,浓度大,反应速率快,温度高于T0℃时,反应物浓度减少,反应速率降低,温度对反应速率的影响不及浓度的影响,
故答案为:高铈离子被还原的反应,正反应为放热反应,开始反应时,反应物浓度大,反应速率快,正反应为放热反应,温度逐渐升高,反应速率加快,温度高于T0℃时,反应物的浓度减少,反应速率减小,温度对反应速率的影响不及浓度的影响.
点评 本题主要考查温度对反应速率的影响,对学生的分析能力和逻辑推理能力有一定的要求,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | Y、Z的氧化物都有两性 | |
| B. | 气态氢化物的稳定性:Z>X | |
| C. | 原子半径:W>Y>Z>X | |
| D. | 最高价氧化物对应水化物的碱性:W<Y |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
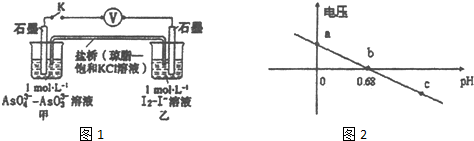
| A. | pH=5 时,负极电极反应式为2I--2e-═I2 | |
| B. | b点时,反应处于化学平衡状态 | |
| C. | a点时,盐桥中K+向左移动 | |
| D. | pH>0.68时,氧化性I2>AsO43- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
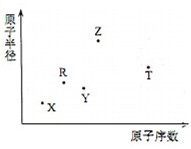 短周期主族元素X、Y、Z、R、T的原子半径与原子序数关系如图所示.R原子最外层电子数是电子层数的2倍.Y与Z能形成Z2Y、Z2Y2型离子化合物.Z与T形成的化合物Z2T能破坏水的电离平衡.下列推断正确的是( )
短周期主族元素X、Y、Z、R、T的原子半径与原子序数关系如图所示.R原子最外层电子数是电子层数的2倍.Y与Z能形成Z2Y、Z2Y2型离子化合物.Z与T形成的化合物Z2T能破坏水的电离平衡.下列推断正确的是( )| A. | 原子半径和离子半径均满足:Y<Z | |
| B. | 氢化物的沸点不一定是:Y>R | |
| C. | 最高价氧化物对应水化物的酸性:T<R | |
| D. | 由X、R、Y、Z四种元素组成的化合物水溶液一定显碱性 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
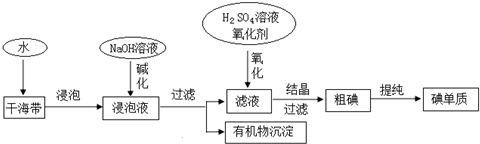
| A. | 因海水中蕴藏着极其丰富的碘元素,所以工业上也可以直接用海水来提取碘元素 | |
| B. | 碱化操作时,加入NaOH溶液的原因是在碱性溶液中,可溶性有机质可形成沉淀 | |
| C. | 在实验室进行氧化操作时,加入的氧化剂可以是新制氯水、双氧水等 | |
| D. | 在实验室进行过滤操作时,需要用到玻璃仪器有玻璃棒、烧杯、漏斗 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 实验步骤 | 预期现象及结论 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题


查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com