
【题目】现有A、B、C、D、E五种短周期元素,已知A、B、C、D四种元素的核内质子数之和为56,在元素周期表中的位置如图所示,1 mol E的单质可与足量酸反应,能产生33.6 L H2(在标准状况下);E的阳离子与A的阴离子核外电子层结构相同。
A | ||
B | C | D |
回答下列问题:
(1)写出下列元素名称A__________,B___________,E____________
(2)C的简单离子结构示意图为_____________
(3)B单质在A单质中燃烧,反应现象是__________________________________,生成物的化学式为___________
(4)A与E形成的化合物的化学式为__________,它的性质决定了它在物质的分类中应属于__________________
(5)向D与E形成的化合物的水溶液中滴入烧碱溶液至过量,此过程中观察到的现象是_______________________,写出有关化学反应方程式______________________________。
【答案】 氧 磷 铝 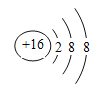 剧烈燃烧,有大量白烟 P2O5 Al2O3 两性氧化物 先出现白色沉淀,继续滴加,白色沉淀溶解 AlCl3 + 3NaOH == Al(OH)3↓ + 3NaCl,Al(OH)3 + NaOH == NaAlO2 + 2H2O
剧烈燃烧,有大量白烟 P2O5 Al2O3 两性氧化物 先出现白色沉淀,继续滴加,白色沉淀溶解 AlCl3 + 3NaOH == Al(OH)3↓ + 3NaCl,Al(OH)3 + NaOH == NaAlO2 + 2H2O
【解析】试题分析:现有A、B、C、D、E五种短周期元素,设C的原子序数为x,根据4种元素在元素周期表中的位置可知,A、B、D的原子序数分别为x-8、x-1、x+1,因为A、B、C、D四种元素的核内质子数之和为56,则有4x-8=56,x=16,所以A、B、C、D分别为O、P、S、Cl。1 mol E的单质可与足量酸反应,能产生33.6 L H2(在标准状况下),氢气的物质的量为1.5mol,则电子转移3mol,E为第IIIA族元素,E的阳离子与O元素的阴离子核外电子层结构相同,则E为Al元素。
(1)A、B、E的元素名称分别为氧、磷、铝;
(2)C的简单离子结构示意图为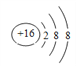 ;
;
(3)磷在氧气中燃烧,反应现象是:剧烈燃烧,有大量白烟,生成物的化学式为P2O5;
(4)O与Al形成的化合物的化学式为Al2O3,氧化铝既能与酸反应又能与碱反应生成盐和水,这决定了它在物质的分类中属于两性氧化物;
(5)向氯化铝的水溶液中滴入烧碱溶液至过量,此过程中观察到的现象是先出现白色沉淀,继续滴加,白色沉淀溶解,有关化学反应方程式为AlCl3 + 3NaOH == Al(OH)3↓ + 3NaCl、Al(OH)3 + NaOH == NaAlO2 + 2H2O。


科目:高中化学 来源: 题型:
【题目】三硫化四磷用于制造火柴即火柴盒摩擦面,分子结构如图所示。下列有关三硫化四磷的说法正确的是( )
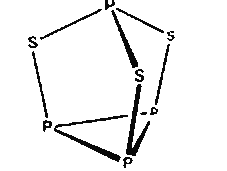
A. 该物质中磷元素的化合价为+3
B. 22 g P4S3含硫原子数目约为1.806×1023
C. 该物质分子结构中S、P最外层电子数均不为8
D. 该物质分子中全是极性共价键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在4L密闭容器中充入6molA气体和5molB气体,一定条件下发生反应:3A(g)+B(g)![]() 2C(g)+xD(g),达到平衡时,生成了2molC,经测定,D的浓度为0.5mol/L,下列判断正确的是
2C(g)+xD(g),达到平衡时,生成了2molC,经测定,D的浓度为0.5mol/L,下列判断正确的是
A. B的转化率为20%
B. 平衡时A的浓度为1.50mol/L
C. x=1
D. 达到平衡时,在相同温度下容器内混合气体的压强是反应前的85%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏伽德罗常数的值,下列叙述正确的是( )
A.0.1molCl2常温下与过量稀NaOH溶液反应转移电子总数为0.1NA
B.25℃时,pH=13的1.0L Ba(OH)2溶液中含有的OH﹣数目为0.2NA
C.标准状况下,22.4LCHCl3含有的分子数为NA
D.1L 0.1molL﹣1的硫化钠溶液中硫离子数目为0.1NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】五种短周期主族元素的部分信息如下表所示:
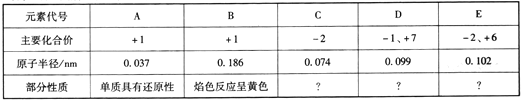
(1)E在元素周期表中的位置是____________________。
(2)在BDC溶液中滴加酚酞溶液,溶液先变红后褪色,原因是__________________(用离子方程式表示)。
(3)25℃时,pH均为10的BCA溶液和B2E溶液中,水电离出的c(OH-)之比为____________。
(4)下列事实中,能说明D的非金属性比E强的是________ (填字母)。
a.D的简单氢化物比E的稳定 b.AD的酸性比A2E的强
c.D的单质的沸点低于E的单质 d.D2与A2E能发生置换反应
(5)500℃时,向容积为1L的恒容密闭容器中充入2mol EC3气体,在催化剂作用下发生反应,经过10min恰好达到平衡,测得平衡浓度c(C2)=0.75mol·L-1。
①反应从开始到平衡时的平均反应速率v(EC2)=____________。
②EC3的平衡转化率为____________。
③其他条件不变,再向容器中充入少量EC3气体,则EC3的平衡转化率会________ (填“增大”“减小”或“不变”)。
(6)在B2E2C3溶液中滴加BAEC4溶液,会析出黄色沉淀并逸出刺激性气体,反应的离子方程式为____________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种气态烷烃和一种气态烯烃组成的混合气体共10g,其密度是相同条件下H2的12.5倍,该混合气通过Br2水时,Br2水增重8.4g,则组成该混合气的可能是( )
A.甲烷、乙烯
B.丙烷、乙烯
C.乙烷、丙烯
D.甲烷、丙烯
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com