��������Ҫ�Ļ���ԭ��
��1����֪��N
2��g��+O
2��g��=2NO��g����H=+180.5kJ?mol
-14NH
3��g��+5O
2��g��=4NO��g��+6H
2O��g����H=-905kJ?mol
-12H
2��g��+O
2��g��=2H
2O��g����H=-483.6kJ?mol
-1д�������ڸ��¸�ѹ�������������ɵ������������Ȼ�ѧ����ʽ��
�������1L�ܱ������У�3mol NH
3 �ڵ��������³�ַ�Ӧ��ƽ��ʱ�ķ�Ӧ��Ϊ92.4kJ�������¶Ȳ��䣬����ʼNH
3�����ʵ�������Ϊ8mol��ƽ��ʱNH
3��ת����Ϊ
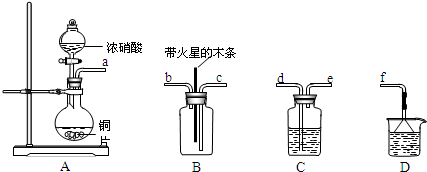
��2�������ڴ�����ȼ�գ�����һ�ֵ��ʺ�ˮ����д���÷�Ӧ�Ļ�ѧ����ʽ��
����ѧ�����ô�ԭ������Ƴɰ���һ����ȼ�ϵ�أ���ͨ�백���ĵ缫��
����������������������������£��õ缫������Ӧ�ĵ缫��ӦʽΪ
��
��3��һ�������£�ij�ܱ������з�����Ӧ��4NH
3��g��+5O
2��g��?4NO��g��+6H
2O��g������һ��������ܱ������У�Ϊʹ�÷�Ӧ�ķ�Ӧ����������ƽ��������Ӧ�����ƶ������д�ʩ�пɲ��õ���
������ĸ���ţ���
a������ѹǿ b���ʵ������¶� c������O
2��Ũ�� d��ѡ���Ч����
��4�����ij��ˮ�ĵ���̶�Ϊ1%��Ũ��Ϊ0.01mol/LMgCl
2��Һ�μӰ�ˮ����ʼ��������ʱ����������Һ����仯������Һ�е�NH
3?H
2O��Ũ��Ϊ
{��֪Ksp[Mg��OH��
2]=4.0��10
-12]}��




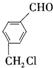
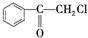 ����Ϊͬ���칹�壬���ܷ���������Ӧ�������к��б�����������-CH3�Ļ������ж��֣����ǵĽṹ��ʽ��
����Ϊͬ���칹�壬���ܷ���������Ӧ�������к��б�����������-CH3�Ļ������ж��֣����ǵĽṹ��ʽ��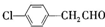 ��
��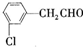 ��
�� ��
�� ������
������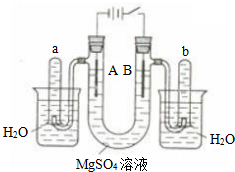 ��ͼ��һ���ò�˿���缫�����ϡ��MgSO4��Һ��װ�ã����Һ�м������Ժ�ָʾ������ʱ��Һ�ʺ�ɫ����ָʾ����pH��ɫ��Χ��6.8��8.0����ɫ-��ɫ����ɫ-��ɫ����
��ͼ��һ���ò�˿���缫�����ϡ��MgSO4��Һ��װ�ã����Һ�м������Ժ�ָʾ������ʱ��Һ�ʺ�ɫ����ָʾ����pH��ɫ��Χ��6.8��8.0����ɫ-��ɫ����ɫ-��ɫ����