
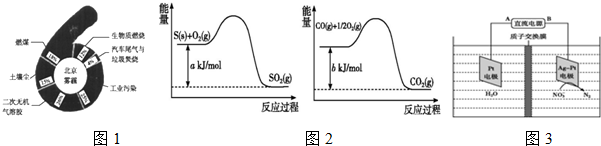
分析 (1)A.反应是可逆反应,不能进行彻底;
B.尾气温度已经很高,再升高温度的意义不大;
C.从平衡常数分析反应进行程度,净化设备经济效益分析;
D.提高净化速率的最好方法是使用高效催化剂;
(2)依据图象书写热化学方程式,
图1:S(s)+O2(g)=SO2(g)△H1=-aKJ/mol
图2 CO(g)+$\frac{1}{2}$O2(g)=CO2(g)△H2=-bKJ/mol;
依据盖斯定律②×2-①得到所需热化学方程式;
(3)发生的化学反应是:2NH3(g)+NO(g)+NO2(g)$?_{催化剂}^{180℃}$2N2(g)+3H2O(g)△H<0,反应是气体体积增大的放热反应,为提高氮氧化物的转化率可采取的措施为:使化学平衡向正反应方向移动可以提高氮氧化物的转化率;
(4)根据二氧化氮具有氧化性,能氧化Na2SO3生成Na2SO4,本身被还原成氮气,方程式为2NO2+4Na2SO3═N2+4Na2SO4,由2NO+ClO2+H2O═NO2+HNO3+2HCl,2NO2+4Na2SO3═N2+4Na2SO4,通过化学方程式建立关系式然后计算;
(5)由N2O4制取N2O5需要是失电子,所以N2O5在阳极区生成,Pt为阳极,A为电源正极,B为电源负极,依据电解原理可知,在阴极反应是NO3-得电子发生还原反应生成N2,阳极反应为H2O失电子氧化为O2和H+.
解答 解:(1)A.该反应为可逆反应,不能完全转化,排出的气体中一定含有NO或CO,故A错误;
B.尾气温度已经很高,再升高温度,反应速率提高有限,且消耗更多能源,意义不大,故B错误;
C、因平衡常数已经较大,增大压强虽然平衡正向移动,但对设备要求更高,不符合生成经济效益,故C错误;
D、研制高效催化剂可提高反应速率,解决反应极慢的问题,有利于尾气的转化,故D正确;
故答案为:D;
(2)图1:S(s)+O2(g)=SO2(g)△H1=-aKJ/mol
图2 CO(g)+$\frac{1}{2}$O2(g)=CO2(g)△H2=-bKJ/mol;
依据盖斯定律②×2-①得到:SO2(g)+2CO(g)=S(s)+CO2(g)△H=2△H2-△H1=-(2b-a)KJ/mol,
故答案为:SO2(g)+2CO(g)=S(s)+2CO2(g)△H=-(2b-a)kJ•mol-1;
(3)使化学平衡向正反应方向移动可以提高氮氧化物的转化率,增加反应物浓度平衡正向移动,所以可以采取增大NH3浓度的措施,由于此反应为放热反应,降低温度平衡正向移动,此反应正反应方向为气体体积增大的方向,减小压强平衡正向移动,
故答案为:增大NH3浓度(或减小压强、降低温度);
(4)二氧化氮具有氧化性,能氧化Na2SO3生成Na2SO4,本身被还原成氮气,方程式为2NO2+4Na2SO3═N2+4Na2SO4,由2NO+ClO2+H2O═NO2+HNO3+2HCl,2NO2+4Na2SO3═N2+4Na2SO4得:
4NO~N2
30×4g 22.4L
60g 11.2L
所以共消耗NO质量60g,
故答案为:2 NO2+4SO32-=N2+4SO42-; 60;
(5)由图示知在Ag-Pt电极上NO3-发生还原反应,因此Ag-Pt电极为阴极,则B为负极,A为电源正极,在阴极反应是NO3-得电子发生还原反应生成N2,利用电荷守恒与原子守恒知有H2O参与反应且有水生成,所以阴极上发生的电极反应式为:2NO3-+6H2O+10e-=N2↑+12OH-,阳极反应为H2O失电子氧化为O2和H+,电极方程式为:2H2O-4e-═4H++O2↑,
故答案为:B;2NO3-+6H2O+10e-=N2↑+12OH-;2H2O-4e-=O2↑+4H+.
点评 本题涉及热化学方程式的计算、化学平衡移动、电解原理、氧化还原原理等知识点,题目综合性程度一般,难度较大,掌握好原理是关键.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
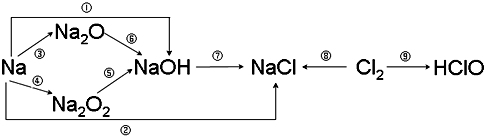
| A. | 反应物的总能量高于生成物的总能量 | |
| B. | 断开1mol H-H键和1 mol I-I键所需能量大于断开2mol H-I键所需能量 | |
| C. | 断开2mol H-I键所需能量约为(c+b+a)kJ | |
| D. | 向密闭容器中加入2 mol H2和2 mol I2,充分反应后放出的热量小于2akJ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
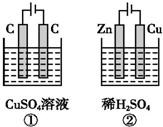 如图所示的两个实验装置中,溶液的体积均为 200mL,开始时电解质溶液的浓度均为 0.1mol•L-1,工作一段时间后,测得两端导线中均通过0.02mol电子,若不考虑盐的水解和溶液体积的变化,则下列叙述中正确的是( )
如图所示的两个实验装置中,溶液的体积均为 200mL,开始时电解质溶液的浓度均为 0.1mol•L-1,工作一段时间后,测得两端导线中均通过0.02mol电子,若不考虑盐的水解和溶液体积的变化,则下列叙述中正确的是( )| A. | 产生气体的总体积:①>② | |
| B. | 电极上析出物质的总质量:②>① | |
| C. | 溶液的pH变化:①增大,②减小 | |
| D. | ①中阳极的电极反应式:4OH--4e-═2H2O+O2↑;②中阴极的电极反应式:2H++2e-═H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 反应①中的两种物质互为同素异形体 | |
| B. | 反应②中HCNO是氧化剂 | |
| C. | 反应②中N2既是氧化产物,又是还原产物 | |
| D. | 反应②中NO2是还原剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com