
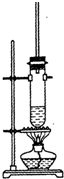
 1-丁醇和乙酸在浓硫酸作用下,通过酯化反应制得乙酸丁酯,反应温度为115-125℃,反应装置如图.下列对该实验的描述中错误的是( )
1-丁醇和乙酸在浓硫酸作用下,通过酯化反应制得乙酸丁酯,反应温度为115-125℃,反应装置如图.下列对该实验的描述中错误的是( )| A. | 提纯乙酸丁酯需要经过水、氢氧化钠溶液洗涤 | |
| B. | 长玻璃管起冷凝回流作用 | |
| C. | 不能用水浴加热 | |
| D. | 加入过量乙酸可以提高1一丁醇的转化率 |
分析 A.用氢氧化钠洗乙酸丁酯,会使乙酸丁酯水解;
B.有机物易挥发,长导管可起冷凝作用;
C.水浴,反应温度不超过100℃,该反应的温度为115~125℃;
D.增加一种反应物浓度,可以提高另一种反应物的转化率.
解答 解:A.提纯乙酸丁酯需使用碳酸钠溶液,吸收未反应的乙酸,溶解丁醇,降低乙酸丁酯的溶解度,如果用氢氧化钠,会使乙酸丁酯水解,故A错误;
B.实验室制取乙酸丁酯,原料乙酸和丁醇易挥发,当有易挥发的液体反应物时,为了避免反应物损耗和充分利用原料,要在发生装置设计冷凝回流装置,使该物质通过冷凝后由气态恢复为液态,从而回流并收集;实验室可通过在发生装置安装长玻璃管或冷凝回流管等实现,故B正确;
C.实验室制取乙酸丁酯,反应需要反应温度为115~125℃,而水浴加热适合温度低于100℃的反应,故C正确;
D.酯化反应为可逆反应,增加乙酸的量,可使平衡向生成酯的方向移动,从而提高1-丁醇的转化率,故D正确;
故选A.
点评 本题考查了乙酸的酯化反应,题目难度中等,掌握乙酸乙酯的制取是类推其他酯的制取的基础,可以根据装置中各部分的作用及酯的性质进行解答.


科目:高中化学 来源: 题型:填空题
 教材中给出了Na2O2与H2O反应的化学方程式2Na2O2+2H2O═4NaOH+O2↑.为了探究Na2O2与H2O反应的机理,某学习探究小组在教师指导下设计了如图装置进行实验.
教材中给出了Na2O2与H2O反应的化学方程式2Na2O2+2H2O═4NaOH+O2↑.为了探究Na2O2与H2O反应的机理,某学习探究小组在教师指导下设计了如图装置进行实验.查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 淀粉与纤维素互为同分异构体 | |
| B. | 汽油、柴油属于纯净物,有固定的熔沸点 | |
| C. | 利用油脂在碱性条件下的水解,可以制甘油和肥皂 | |
| D. | 蛋白质属于天然高分子化合物,盐酸可以使蛋白质变黄,称为颜色反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 (1)与明矾相似,硫酸铁也可用作净水剂,其原理为Fe3++3H2O???Fe(OH)3(胶体)+3H+(用离子方程式表示).
(1)与明矾相似,硫酸铁也可用作净水剂,其原理为Fe3++3H2O???Fe(OH)3(胶体)+3H+(用离子方程式表示).查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C15H27COOH | B. | C16H29COOH | C. | C17H31COOH | D. | C17H33COOH |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2 | B. | NH4NO3$\frac{\underline{\;△\;}}{\;}$N2O↑+2H2O | ||
| C. | 2NaHCO3$\frac{\underline{\;△\;}}{\;}$Na2CO3+CO2↑+H2O | D. | CuO+CO═Cu+CO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
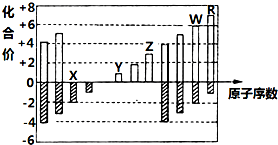 如图是部分短周期元素主要化合价与原子序数的关系图(X、Y、Z、W、R代表五种元素符号).下列说法中正确的是( )
如图是部分短周期元素主要化合价与原子序数的关系图(X、Y、Z、W、R代表五种元素符号).下列说法中正确的是( )| A. | 原子半径比较:Z>Y>X | |
| B. | 最高价氧化物对应的水化物的酸性比较:W>R | |
| C. | X和Y形成的化合物中只含离子键 | |
| D. | Z的氧化物和Y的 最高价氧化物对应的水化物能反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com