
下列说法正确的是
A. pH<7.0的降水通常称为酸雨 B. 燃煤时加入适量石灰石,可减少废气中SO2的量
C. 新制氯水经光照一段时间酸性减弱 D. 测定氯水的pH应用干燥的pH试纸,不能用蒸馏水润湿
 名牌学校分层周周测系列答案
名牌学校分层周周测系列答案 黄冈海淀全程培优测试卷系列答案
黄冈海淀全程培优测试卷系列答案科目:高中化学 来源:2017届吉林省高三第五次摸底考试理综化学试卷(解析版) 题型:选择题
分子式为C4H8ClBr的有机物共有(不含立体异构)
A. 9种 B. 10种 C. 11种 D. 12种
查看答案和解析>>
科目:高中化学 来源:2017届山东省济南市高三第一次模拟考试理科综合化学试卷(解析版) 题型:简答题
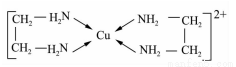
GaN、GaP、GaAs是人工合成的一系列新型半导体材料,其晶体结构均与金刚石相似。铜是重要的过渡元素,能形成多种配合物,如Cu2+与乙二胺(H2N-CH2-CH2-NH2)可形成如图所示配离子。回答下列问题:
(1)基态Ga原子价电子的轨道表达式为________________;
(2)熔点:GaN_____GaP(填“>”或“<”);
(3)第一电离能:As_____Se(填“>”或“<”);
(4)Cu2+与乙二胺所形成的配离子内部不含有的化学键类型是______;
a.配位键 b.极性键 c.离子键 d.非极性键
(5)乙二胺分子中氮原子轨道的杂化类型为________,乙二胺和三甲胺[N(CH3)3]均属于胺。但乙二胺比三甲胺的沸点高很多,原因是___________;
(6)Cu的某种晶体晶胞为面心立方结构,晶胞边长为acm,铜原子的半径为rcm。该晶体中铜原子的堆积方式为_______型(填“A1”、“A2”或“A3”),该晶体密度为____g/cm3(用含a和NA的代数式表达),该晶体中铜原子的空间利用率为______(用含a和r的代数式表达)。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江西省南昌市高一下学期第一次月考化学试卷(解析版) 题型:选择题
将盛有12mLNO2和O2混合气体的量筒倒立于水槽中,充分反应后,还剩余2mL无色气体,则原混合气体中O2的体积可能是( )

A.2.1mL B.2.4mL C.3.6mL D.4mL
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江西省南昌市高一下学期第一次月考化学试卷(解析版) 题型:选择题
取三个干燥的烧瓶,分别装入标准状况下的干燥氨气、含有二分之一体积空气的氯化氢、二氧化氮和氧气(体积比为4∶1)的混合气体;然后分别做溶解于水的喷泉实验。实验结束后三个烧瓶中所得溶液的物质的量浓度之比为( )
A.2∶1∶2 B.1∶1∶1
C.5∶5∶4 D.7∶7∶4
查看答案和解析>>
科目:高中化学 来源:宁夏勤行校区2016-2017学年高二下学期第一次(3月)月考化学试卷 题型:简答题
现有部分元素的性质或原子结构信息如表,据此回答下列问题:
元素编号 | 元素性质或原子结构 |
T | M层上有2对成对电子 |
X | 最外层电子数是次外层电子数的2倍 |
Y | 常温下单质为双原子分子,其氢化物的水溶液显碱性 |
Z | 短周期元素最高正化合价是+7价 |
W | 3d能级电子数是最外层电子数的3倍 |
(1)元素X的基态原子核外共有________种空间运动状态不同的电子,元素X与H元素形成的化合物是当今重要的能源,该化合物的电子式为________。
(2)元素Y的价电子排布图为________________,元素Y与元素T相比,电负性较大的是________(用元素符号表示)。
(3)元素Z与元素T相比,非金属性强的是________(用元素符号表示),下列表述中能证明这一事实的是________。
a.常温下Z的单质和T的单质状态不同
c.一定条件下Z和T的单质都能与氢氧化钠溶液反应
b.Z的氢化物比T的氢化物稳定
d.最高价氧化物对应水化物的酸性Z的比T的酸性强
(4)W的价电子排布式为________,稳定性比较:W3+________W2+(填“>”或“<”),原因是__________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源:宁夏勤行校区2016-2017学年高二下学期第一次(3月)月考化学试卷 题型:选择题
已知由三种元素构成的四种物质存在下列反应,其中a的分子空间构型为正四面体。组成a分子的两种元素的原子序数和小于10,组成b分子的元素为第三周期的元素。则下列判断正确的是
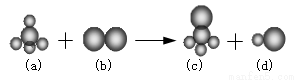
A.四种分子中的化学键均是极性键 B.a、c分子中中心原子均为sp3杂化
C.四种分子中既有σ键,又有π键 D.b、d分子中共价键的键能b大于d
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山西省大同市高二3月月考化学试卷(解析版) 题型:简答题
第ⅥA族的氧、硫、硒、碲等元素在化合物中常表现出多种氧化态,含ⅥA族元素的化合物在研究和生产中有许多重要用途。请回答下列问题:
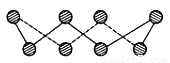
(1)S单质的常见形式为S8,其环状结构如下图所示,S原子采用的轨道杂化方式是_____;
(2)原子的第一电离能是指气态电中性基态原子失去一个电子转化为气态基态正离子所需要的最低能量,O、S、Se原子的第一电离能由大到小的顺序为_______;
(3)Se原子序数为____,其核外M层电子的排布式为____;
(4)H2Se的酸性比H2S___(填“强”或“弱”)。气态SeO3分子的立体构型为___,SO32-离子的立体构型为______;SO32-离子中S原子的杂化方式为____________。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年重庆第二外国语学校高一下学期3月份月考化学试卷(解析版) 题型:选择题
下列有关元素周期表中元素性质的叙述不正确的是( )
A. 同主族元素从上到下,非金属性逐渐减弱
B. 元素的最高正化合价在数值上均等于原子的最外层电子数
C. 同周期元素的原子半径从左到右逐渐减小(稀有气体除外)
D. 元素的非金属性越强,它的最高价氧化物的水化物的酸性越强
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com