
A.C—H B.Si—H C.P—H D.S—H
 53天天练系列答案
53天天练系列答案科目:高中化学 来源: 题型:



查看答案和解析>>
科目:高中化学 来源: 题型:



查看答案和解析>>
科目:高中化学 来源:三点一测丛书 高中化学 必修2 (江苏版课标本) 江苏版课标本 题型:043
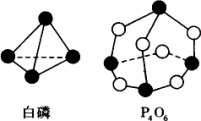
化学反应可视为旧键断裂和新键形成的过程,化学键的键能是形成(或拆开)1 mol化学键时释放出(或吸收)的能量.已知白磷和P4O6的分子结构如图所示,现提供以下化学键的键能(kJ·mol-1)P-P:198 P-O:360 O-O:498计算反应P4(白磷)+3O2→P4O6的反应热为________.
PCl5也是一种白色固体,加热到160℃不经过液态阶段就变为蒸气,测得180℃下的蒸气密度(折合成标准状况)为9.3 g·L-1,继续加热到250℃时测得压力为计算值的两倍.PCl5在加压下于148℃液化,形成一种能导电的液体,测得P-Cl的键长为198 pm和206 pm两种.根据以上条件回答下列问题:
(1)PCl5固体是一种什么类型的晶体?180℃下PCl5蒸气中存在什么分子?为什么?
(2)250℃下PCl5蒸气中存在什么分子?为什么?
(3)PCl5熔体为什么导电?用最简洁的形式作出解释?
查看答案和解析>>
科目:高中化学 来源:2012-2013学年河南省六市高三第二次联考化学试卷(解析版) 题型:填空题
铜在我国有色金属材料的消费中仅次于铝,广泛地应用于电气、机械制造、国防等领域。请回答下列问题:
(1)青铜的主要组成元素是铜元素和锡元素,请写出锡原子的价电子排布式 。
(2)向硫酸铜溶液里滴加氨水至过量,再加入乙醇,析出晶体,此物质中含有的化学键类型为 ,SO2—4的立体构型是 ,其中S原子的杂化轨道类型是 。
(3)N、O、F三种元素的电负性由大到小的顺序为 ,Cu2O的熔点高于Cu2S,请解释原因: 。
(4)金属铜单独与氨水或单独与过氧化氢都不能反应,但可与氨水和过氧化氢的混合溶液反应,反应的化学方应程式为 。
(5)用晶体的x射线衍射法可以测得阿伏加德罗常数。对金属铜的测定得到以下结果:晶胞为面心立方最密堆积,边长为361pm。又知铜的密度为9.00g.cm-3,据此计算阿伏加德罗常数为 [列式并计算,结果用科学记数法表示,保留两位小数,己知Ar(Cu)=63.6]。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com